Chemische hybridisatie sp, sp2, sp3
de chemische hybridisatie is het "mengsel" van de atomaire orbitalen, waarvan het concept werd geïntroduceerd door de chemicus Linus Pauling in 1931 om de onvolkomenheden van de Theorie van de Link van Valencia (TEV) te dekken. Welke fouten? Dit zijn: de moleculaire geometrie en lengtes equivalente bindingen in moleculen zoals methaan (CH4).
Volgens TEV vormen de atomaire orbitalen van C in methaan vier σ-bindingen met vier H-atomen.De 2p-orbitalen met formasevormen (onderbeeld) van C staan loodrecht op elkaar, dus de Hs moeten uit elkaar worden gehouden onder een hoek van 90 °.
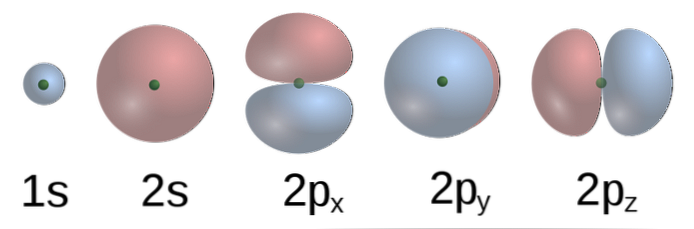
Bovendien is de 2s (sferische) orbitaal van C gekoppeld aan de 1s orbitaal van de H onder een hoek van 135º ten opzichte van de andere drie Hs. Er is echter experimenteel gevonden dat de hoeken in de CH4 zijn 109,5º en bovendien zijn de lengtes van de C-H-bindingen equivalent.
Om dit te verklaren, moet een combinatie van de oorspronkelijke atoomorbitalen worden beschouwd als vier gedegenereerde hybride orbitalen (van gelijke energie). Hier komt chemische chemie. Hoe zien hybride orbitalen eruit? Het hangt af van de atomaire orbitalen die ze genereren. Ze vertonen ook een mengsel van de elektronische kenmerken hiervan.
index
- 1 sp3 hybridisatie
- 1.1 Interpretatie
- 1.2 Afwijkingen van de hoeken van schakels
- 2 Hybridisatie sp2
- 3 Hybridisatie sp
- 4 Referenties
Hybridisatie sp3
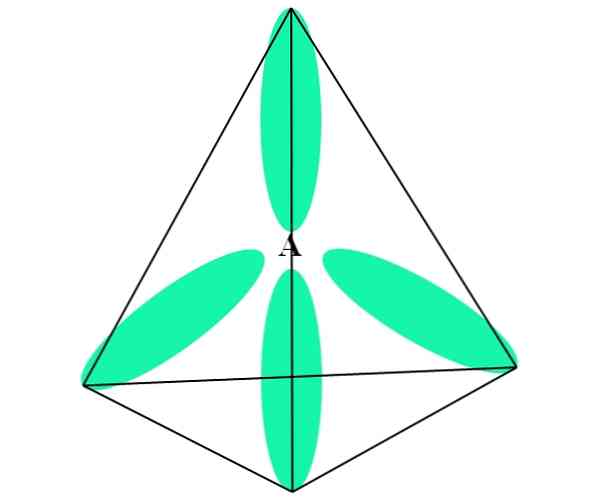
In het geval van CH4, Hybridisatie van C is sp3. Vanuit deze benadering wordt de moleculaire geometrie uitgelegd met vier sp-orbitalen3 gescheiden bij 109,5º en wijzend naar de hoekpunten van een tetraëder.
In de bovenstaande afbeelding kun je zien hoe de sp-orbitalen3 (groen) vestigen een tetraëdrische elektronische omgeving rondom het atoom (A, dat is C voor de CH4).
Waarom 109,5º en geen andere hoeken, om een andere geometrie te "tekenen"? De reden is dat deze hoek de elektronische afstoting van de vier atomen minimaliseert die aan A zijn gekoppeld.
Op deze manier is het CH-molecuul4 kan worden weergegeven als een tetraëder (tetraedrische moleculaire geometrie).
Als, in plaats van H, C verbindingen met andere groepen atomen vormt, wat zou dan de hybridisatie ervan zijn? Zolang de koolstof vier σ-bindingen (C-A) vormt, zal zijn hybridisatie dat wel zijn3.
Er kan worden aangenomen dat in andere organische verbindingen zoals CH3OH, CCl4, C (CH3)4, C6H12 (cyclohexaan), etc., heeft de koolstof een sp-hybridisatie3.
Dit is van fundamenteel belang voor het schetsen van organische structuren, waarbij koolstoffen met eenvoudige bindingen punten van divergentie vertegenwoordigen; dat wil zeggen, de structuur blijft niet in een enkel vlak.
interpretatie
Wat is de eenvoudigste interpretatie voor deze hybride orbitalen zonder de wiskundige aspecten (de golffuncties) aan te pakken? De sp orbitalen3 impliceren dat ze zijn ontstaan door vier orbitalen: één en drie p.
Omdat de combinatie van deze atomaire orbitalen ideaal zou moeten zijn, de vier sp-orbitalen3 resulterende zijn identiek en bezetten verschillende oriëntaties in de ruimte (zoals in de orbitalen pX, pen en pz).
Het bovenstaande is van toepassing op de rest van de mogelijke hybridisaties: het aantal hybride orbitalen dat wordt gevormd is hetzelfde als dat van de gecombineerde atomaire orbitalen. Bijvoorbeeld sp hybride orbitalen3d2 ze zijn gevormd uit zes atomaire orbitalen: één, drie p en twee d.
Afwijkingen van de hoeken van schakels
Volgens de theorie van afstoting van de elektronische paren van de laag Valencia (VSEPR), bezet een paar vrije elektronen meer volume dan een gekoppeld atoom. Dit zorgt ervoor dat de koppelingen uit elkaar gaan, waardoor de elektronische spanning afneemt en de 109,5º-hoeken veranderen:
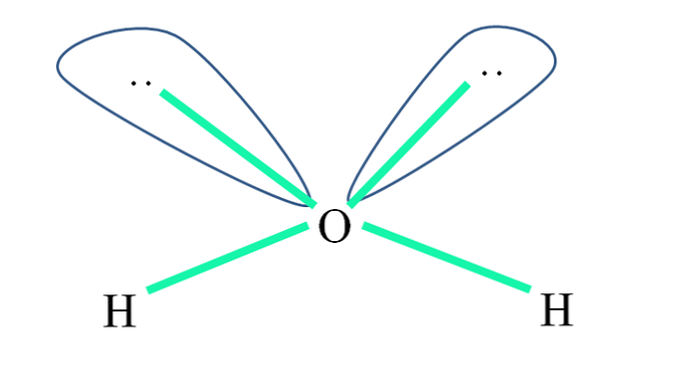
In het watermolecuul zijn de H-atomen bijvoorbeeld gebonden aan de sp-orbitalen3 (in groen), en ook de paren niet-gedeelde elektronen ":" bezetten deze orbitalen.
De repulsies van deze elektronenparen worden meestal weergegeven als "twee bollen met ogen", die, vanwege hun volume, de twee bindingen σ O-H afweren.
Dus in het water zijn de hoeken van schakels in werkelijkheid 105º, in plaats van de 109,5 º die wordt verwacht voor de tetraëdrische meetkunde.
Welke geometrie heeft H dan?2O? Het heeft een hoekige geometrie. Waarom? Omdat, hoewel de elektronische geometrie viervlakkig is, twee paren niet-gedeelde elektronen hiervan afleiden tot een hoekige moleculaire geometrie.
Hybridisatie sp2
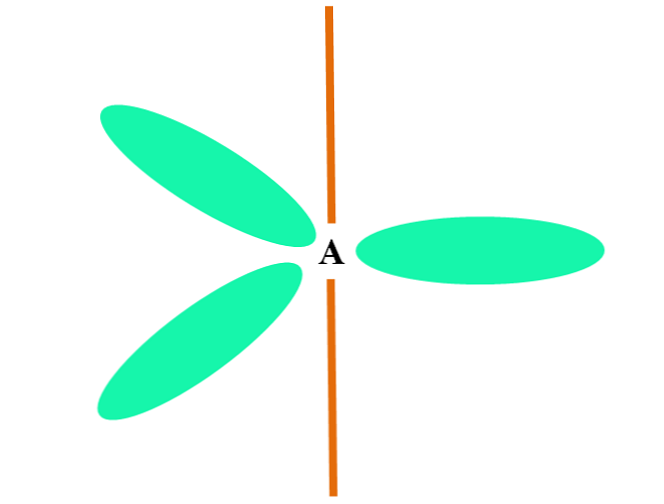
Wanneer een atoom twee p en één s orbitalen combineert, genereert het drie sp hybride orbitalen2; een orbitaal p blijft echter ongewijzigd (omdat ze drie zijn), wat in de afbeelding hierboven wordt weergegeven als een oranje balk.
Hier, de drie sp-orbitalen2 ze zijn groen om hun verschil met de oranje balk te benadrukken: de "pure" p-orbitaal.
Een atoom met sp-hybridisatie2 kan worden gevisualiseerd als een platte driehoekige vloer (de driehoek getekend met de sp-orbitalen2 van groene kleur), met zijn hoekpunten gescheiden door 120 ° hoeken en loodrecht op een balk.
En welke rol speelt de pure p-orbitale? Dat van het vormen van een dubbele band (=). De sp orbitalen2 sta de vorming toe van drie σ-bindingen, terwijl de zuivere p-orbitale a π-binding (een dubbele of drievoudige binding impliceert een of twee π-bindingen).
Om bijvoorbeeld de carbonylgroep en de structuur van het formaldehyde-molecuul te tekenen (H.2C = O), gaat als volgt verder:
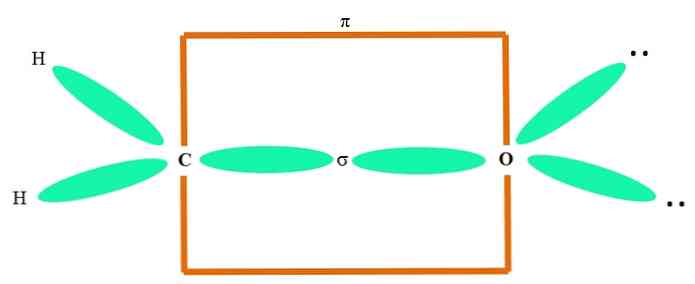
De sp orbitalen2 beide van C en O vormen een binding σ, terwijl hun zuivere orbitalen een binding π vormen (de oranje rechthoek).
Er is te zien hoe de rest van de elektronische groepen (H-atomen en niet-gedeelde elektronenparen) zich in de andere sp-orbitalen bevinden.2, gescheiden door 120º.
Hybridisatie sp
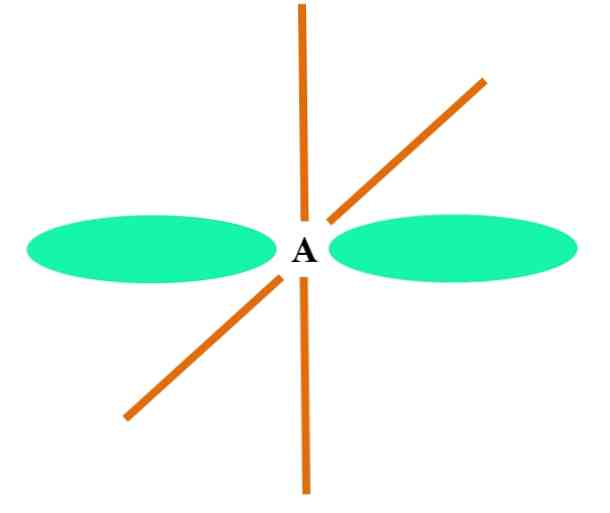
De bovenste afbeelding toont een atoom A met sp-hybridisatie. Hier combineren een orbitale s en een p-orbitaal twee gedegenereerde sp-orbitalen. Nu blijven echter twee pure p-orbitalen ongewijzigd, waardoor A twee dubbele bindingen of een drievoudige binding (≡) kan vormen.
Met andere woorden: als in een structuur een C voldoet aan het bovenstaande (= C = of C≡C), dan is de hybridisatie sp. Voor andere minder illustratieve atomen - zoals overgangsmetalen - is de beschrijving van de elektronische en moleculaire geometrieën gecompliceerd omdat de orbitalen d en zelfs de f orbitalen ook worden beschouwd..
De hybride orbitalen zijn gescheiden door een hoek van 180º. Om deze reden zijn de gekoppelde atomen gerangschikt in een lineaire moleculaire geometrie (B-A-B). Tot slot ziet u in de afbeelding hieronder de structuur van de cyanide-anion:

referenties
- Sven. (3 juni 2006). S-p-orbitalen. [Afbeelding]. Opgehaald op 24 mei 2018, van: commons.wikimedia.org
- Richard C. Banks. (Mei 2002). Bonding en hybridisatie. Opgehaald op 24 mei 2018, uit: chemistry.boisestate.edu
- James. (2018). Een Hybridization Shortcut. Opgehaald op 24 mei 2018, uit: masterorganicchemistry.com
- Dr. Ian Hunt. Afdeling Scheikunde, Universiteit van Calgary. sp3-hybridisatie. Opgehaald op 24 mei 2018, vanaf: chem.ucalgary.ca
- Chemical Bonding II: Molecular Geometry and Hybridization of Atomic Orbitals Hoofdstuk 10. [PDF]. Opgehaald op 24 mei 2018, vanuit: wou.edu
- Quimitube. (2015). Covalente binding: Inleiding tot de hybridisatie van atomaire orbitalen. Opgehaald op 24 mei 2018, vanaf: quimitube.com
- Shiver & Atkins. (2008). Anorganische chemie (Vierde editie, pagina 51). Mc Graw Hill.


