Verzepingsreactie en stoffen die kunnen worden verkregen
de verzeping Het is de basische hydrolyse van een ester. Dit betekent dat de ester onomkeerbaar reageert met een base (NaOH of KOH), waarbij alcohol en carboxylaten van natrium of kalium worden geproduceerd. Het woord betekent "vervaardiging van zepen" en is in feite een van de oudste chemische reacties die door de mensheid worden gebruikt.
In de Babylonische tijden, met de hulp van de as verzameld uit hout en planten en dierlijke vetten, perfectioneerden ze de kunst van het maken van zepen. Waarom dierlijk vet? De reden is dat het rijk is aan glycerol triesters (triglyceriden), en hout as is een bron van kalium, het basismetaal.
Anders gaat de reactie naar een lagere opbrengst, maar voldoende om de effecten ervan op de verf en sommige oppervlakken te weerspiegelen. Dat is het geval bij olieverfschilderijen, waar de pigmenten worden vermengd met olie (bron van esters).
index
- 1 Verzepingsreactie
- 1.1 Mechanisme
- 1.2 Kinetiek
- 2 Stoffen die kunnen worden verkregen door verzeping
- 2.1 Oplosmiddelwerking van zepen
- 3 referenties
Verzepingsreactie
mechanisme
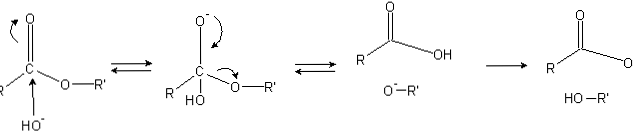
De esters hebben een acylgroep (O = C-R), die gevoelig is voor nucleofiele aanvallen zoals OH-.
Omdat zuurstofatomen elektronische dichtheid van het koolstofatoom "stelen", is het gedeeltelijk geladen, zelfs meer in het geval van esters.
Dientengevolge trekt deze positieve lading negatieve soorten aan die in staat zijn om elektronen aan het koolstofatoom te leveren, waarbij de nucleofiele aanval optreedt (de linkerkant van het beeld). Als een resultaat wordt een tetraedrisch tussenproduct (het tweede molecuul van links naar rechts) gevormd.
De negatieve lading op de zuurstof van het tetraëdrische tussenproduct is het product van een OH- omgeving. Vervolgens wordt deze negatieve lading gedelocaliseerd om de carbonylgroep te laten ontstaan, waardoor de C-OR-binding wordt "verbroken". Ook produceert deze verplaatsing een carbonzuur RCOOH en een alkoxide-ion R'O-.
Tenslotte, als het reactiemedium basisch is, deprotoneert het alkoxide één molecuul water en reageert het carbonzuur met een ander OH- van het medium, het genereren van de producten van verzeping.
kinetica
De snelheid van de verzepingsreactie is evenredig met de concentraties van de reactanten. Met andere woorden, als de concentratie van de ester (RCOOR ') of de base (NaOH) toeneemt, zal de reactie met een hoger tempo verlopen.
Dit wordt ook als volgt vertaald: de verzepingssnelheid is de eerste orde met betrekking tot de ester en de eerste orde met betrekking tot de base. Het bovenstaande kan worden uitgedrukt met de volgende wiskundige vergelijking:
Snelheid = k [RCOOR '] [NaOH]
Waarin k de constante- of snelheidscoëfficiënt is, die varieert als een functie van temperatuur of druk; dat wil zeggen, hoe hoger de warmte, hoe groter de verzepingssnelheid. Om deze reden is het medium onderhevig aan koken.
Omdat beide reagentia van de eerste orde kinetiek zijn, is de algehele reactie de tweede orde.
In het reactiemechanisme van verzeping vereist de vorming van het tetraëdrische tussenproduct de nucleofiele aanval, die zowel de ester als de base omvat.
De kinetiek van de tweede orde wordt dus weerspiegeld in dit feit, omdat ze ingrijpen in de (langzame) determinantstap van de reactie..
Stoffen die kunnen worden verkregen door verzeping

De belangrijkste producten van de verzeping zijn alcoholen en zouten van carbonzuren. In een zuur milieu worden de respectieve RCOOH verkregen door verzeping van vetten en oliën, die bekend staan als vetzuren, verkregen..
Op deze manier bestaan zepen uit zouten van de vetzuren die het gevolg zijn van verzeping. Ga je uit met welke kationen? Ze kunnen Na zijn+, K+, mg2+, geloof3+, etc.
Deze zouten zijn oplosbaar in water, maar neerslaan door de werking van het NaCl dat aan het mengsel wordt toegevoegd, dat de zeep dehydrateert en scheidt van de waterige fase. De verzepingsreactie voor een triglyceride is als volgt:
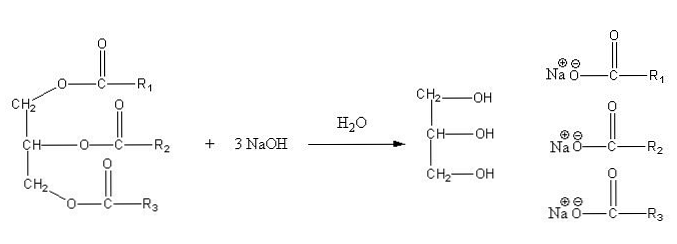
Glycerine is de alcoholische "E" en zeep is alle zouten van de resulterende vetzuren. Hier heeft elke zijketen -R verschillende lengtes en een mate van onverzadiging. Bijgevolg maken deze ketens het verschil tussen vetten en plantaardige oliën.
De sleutel tot de productie van zepen ligt dan in de selectie van de beste vetten en oliën, of meer specifiek in de selectie van verschillende bronnen van triglyceriden.
Deze witte zeepachtige massa kan kleurstoffen en andere organische verbindingen bevatten in zijn structuur, waardoor het aangename aroma's en heldere kleuren krijgt. Vanaf hier wordt het scala van mogelijkheden getemd door kunst en roeping in deze handel.
De verzepingsreactie is echter ook een synthetische route van carbonzuren en alcoholen die niet noodzakelijkerwijs te maken hebben met glycerine of zepen.
Basische hydrolyse van elke ester, zoals eenvoudig ethylacetaat, zal bijvoorbeeld azijnzuur en ethanol produceren.
Oplosmiddelwerking van zepen

De zouten van de vetzuren zijn oplosbaar in water, maar niet op dezelfde manier als de ionen zijn gesolvateerd; dat wil zeggen, omringd door een waterige bol. In het geval van zepen, verhinderen hun zijketens -R dat ze in theorie oplossen in water.
Daarom, om deze energetisch ongemakkelijke positie tegen te gaan, zijn ze zo georiënteerd dat deze kettingen in contact komen, een apolaire organische kern vormen, terwijl de polaire hoofden, het einde (-COO)- na+), interactie met watermoleculen en creëer een "poolschaal".
Het bovenstaande is geïllustreerd in de afbeelding hierboven, waar dit type structuur bekend staat als micelle.
De "zwarte staarten" komen overeen met de hydrofobe kettingen, verstrikt raken in een organische kern beschermd door de grijze bollen. Deze grijze bollen vormen het polaire schild, de koppen -COO- na+.
Vervolgens zijn de micellen clusters (clusters) van de zouten van de vetzuren. Daarbinnen kunnen ze vet omsluiten, dat onoplosbaar is in water vanwege zijn apolaire karakter.
Hoe doen ze het? Zowel de vet- als de -R-ketens zijn hydrofoob, dus beide hebben een grote affiniteit voor elkaar.
Wanneer de micellen de vetten omsluiten, reageert het water met de polaire schil, waardoor de zeep oplosbaar is. Evenzo zijn de micellen negatief geladen, waardoor ze elkaar afstoten en daardoor de verspreiding van het vet genereren.
referenties
- Anne Marie Helmenstine, Ph.D. (3 oktober 2017). Verzeping Definitie en reactie. Opgehaald op 24 april 2018, van: thoughtco.com
- Francis A. Carey. Organische chemie Carbonzuren. (zesde editie., blz. 863-866). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Organische chemie. Lipiden (10e editie., Pagina 1056-1058). Wiley Plus.
- Wikipedia. (2018). Verzeping. Opgehaald op 24 april 2018, vanaf: en.wikipedia.org
- Boyd C. (27 februari 2015). Begrijp de chemie en geschiedenis van zeep. Opgehaald op 24 april 2018, vanaf: chemservice.com
- Luca Laghi (27 maart 2007). Verzeping. Opgehaald op 24 april 2018, van: commons.wikimedia.org
- Amanda Crochet (12 mei 2015). Micelle (grijswaarden). Opgehaald op 24 april 2018, van: commons.wikimedia.org


