Ammoniumsulfaat chemische structuur, eigenschappen en toepassingen
de ammoniumsulfaat Het is een ternair en ammoniakaal anorganisch zout van zwavelzuur. De chemische formule is (NH4)2SW4. Daarom zeggen de stoichiometrische verhoudingen dat voor elk sulfaatanion er twee ammoniumkationen in wisselwerking staan. Dit maakt de neutraliteit van het zout mogelijk ((+1) ∙ 2 + (-2)).
Zijn nomenclatuur is te wijten aan het feit dat het een zout is dat is afgeleid van H2SW4, het achtervoegsel "uric" veranderen in "ato". Dus de twee eerste protonen zijn vervangen door NH4+, reactieproduct met ammoniak (NH3). Vervolgens is de chemische vergelijking voor de synthese ervan: 2 NH3 + H2SW4 => (NH4)2SW4
Ammoniumsulfaat is een stikstof- en zwavelopslag, beide onmisbaar in de chemie van bodem en kunstmest.
index
- 1 Chemische structuur
- 2 Fysische en chemische eigenschappen
- 2.1 Molecuulgewicht
- 2.2 Fysiek uiterlijk
- 2.3 Geur
- 2,4 Smeltpunt
- 2.5 Oplosbaarheid
- 2.6 Dichtheid
- 2.7 Dampspanning
- 2.8 Vlampunt
- 2,9 pH
- 2.10 Stabiliteit
- 2.11 Ontleding
- 2.12 Corrosie
- 3 Gebruik
- 3.1 In de landbouw
- 3.2 Als een analytisch reagens
- 3.3 Bij de precipitatie en isolatie van eiwitten
- 3.4 In de branche
- 3.5 Andere toepassingen
- 4 Referenties
Chemische structuur
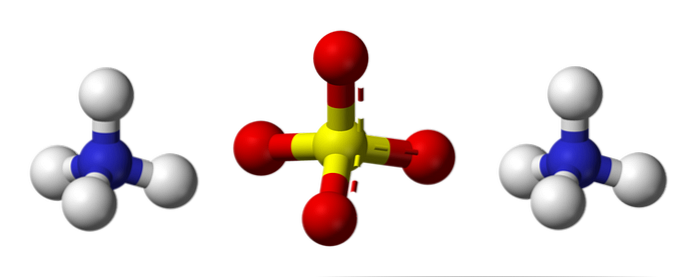
Het bovenste beeld illustreert de moleculaire geometrieën van de NH-ionen4+ en ZO42-. De rode bollen komen overeen met de zuurstofatomen, de witte bollen komen overeen met de waterstofatomen, de blauwe bollen met het stikstofatoom en de gele bollen komen overeen met het zwavelatoom.
Beide ionen kunnen worden beschouwd als twee tetraëders, en hebben dus drie eenheden die samenwerken om een orthorhombische kristalrangschikking te vormen. Het sulfaatanion is SO42- en is in staat om vier waterstofbruggen te doneren of te accepteren, net als het NH-kation4+.
Fysische en chemische eigenschappen
Moleculair gewicht
132.134 g / mol.
Uiterlijke verschijning
Effen wit. Orthorombische witte of bruine kristallen, afhankelijk van verontreinigingsniveaus.
geur
toilet.
Smeltpunt
280 ºC. Dit smeltpunt, laag in vergelijking met andere ionische verbindingen, is te wijten aan het feit dat het een zout is met eenwaardige kationen (+1) en met ongelijksoortige ionen in zijn groottes, waardoor de vaste stof een lage kristallijne reticulaire energie heeft.
oplosbaarheid
76,4 g / 100 g water bij 25 ºC. Deze affiniteit voor water is te danken aan het grote vermogen van zijn moleculen om ammoniumionen te solvateren. Aan de andere kant is het onoplosbaar in aceton en in alcohol; dat wil zeggen, in oplosmiddelen die minder polair zijn dan water.
dichtheid
1,77 g / cm3 bij 25 ºC.
Stoom druk
1.871 kPa bij 20 ºC.
Ontvlambaarheidspunt
26 ºC.
pH
5,0 - 6,0 (25 ° C, 1 M oplossing). De enigszins zure pH is te wijten aan de hydrolyse van NH4+ in water, produceert H3O+ bij lage concentraties.
stabiliteit
Stabiel onder geschikte omgevingsomstandigheden. Contact met sterke oxidatiemiddelen kan vlam vatten.
ontleding
Het begint te ontleden bij 150 ºC, waardoor giftige dampen vrijkomen van zwaveloxide, stikstofoxide en ammonium.
corrosie
Valt geen ijzer of aluminium aan.
toepassingen

In de landbouw
- Ammoniumsulfaat wordt gebruikt als meststof in alkalische bodems. Het ammoniumzout heeft 21% stikstof en 24% zwavel in zijn samenstelling. Er zijn echter verbindingen die een grotere hoeveelheid stikstof verschaffen dan ammoniumsulfaat; Het voordeel van de laatste is de hoge zwavelconcentratie.
- Zwavel is essentieel in de synthese van eiwitten, omdat verschillende aminozuren - zoals cystine, methionine en cysteïne - zwavel bezitten. Om deze redenen blijft ammoniumsulfaat een van de belangrijkste meststoffen.
- Het wordt gebruikt in de gewassen tarwe, maïs, rijst, katoen, aardappelen, hennep en fruitbomen.
- Lage pH van alkalische bodems vanwege hun bijdrage aan het nitrificatieproces uitgevoerd door microben. Ammonium (NH) wordt gebruikt4+) om nitraat te produceren (NO3-) en laat H los+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. De toename in waterstofconcentratie verlaagt de pH van basische bodems en maakt meer gebruik mogelijk.
- Naast het gebruik als meststof, werkt ammoniumsulfaat ook als coadjuvans voor oplosbare insecticiden, herbiciden en fungiciden, die op gewassen worden gesproeid..
- Sulfaat is in staat om in de bodem en in het irrigatiewater aanwezige ionen te sequestreren die nodig zijn voor het leven van bepaalde pathogenen. Onder de ionen die het ammoniumsulfaat vangt zijn de Ca2+, de Mg2+, het geloof2+ en het geloof3+. Deze actie verbetert het microbicide effect van de genoemde middelen.
Als een analytisch reagens
Ammoniumsulfaat werkt als een precipitatiemiddel bij elektrochemische analyse, in microbiologische kweekmedia en bij de bereiding van ammoniumzouten.
Bij de precipitatie en isolatie van eiwitten
Ammoniumsulfaat wordt gebruikt bij de isolatie en zuivering van eiwitten, met name plasma-eiwitten. Een hoeveelheid ammoniumsulfaat wordt aan het plasma toegevoegd tot een bepaalde concentratie; aldus wordt de precipitatie van een groep eiwitten veroorzaakt.
Het precipitaat wordt door centrifugeren verzameld en een additionele hoeveelheid ammoniumsulfaat wordt aan het supernatant toegevoegd en bij een nieuwe concentratie vindt de precipitatie van een andere groep van eiwitten plaats..
De herhaling van het vorige proces in sequentiële vorm maakt het mogelijk om als gevolg daarvan verschillende fracties van plasmaproteïnen te verkrijgen.
Alvorens de nieuwe technologieën van de moleculaire biologie te verschijnen, maakte deze procedure de isolatie mogelijk van plasma-eiwitten die van groot belang zijn in de geneeskunde, bijvoorbeeld: immunoglobulinen, coagulatiefactoren, enz..
In de industrie
Ammoniumsulfaat werkt om het begin van de brand in de textielindustrie te vertragen. Het wordt gebruikt als additief in de galvaniseerindustrie. Het wordt ook gebruikt bij de productie van waterstofperoxide, ammoniumchloride, enz..
Andere toepassingen
- Ammoniumsulfaat wordt gebruikt als een regulerend middel voor osmotische druk en als een zout-precipitatiemiddel.
- In de vorm van ammoniumlaurylsulfaat neemt de oppervlaktespanning van het water af, waardoor de scheiding van verontreinigende stoffen mogelijk wordt door de hardheid van het water te verhogen.
- Het is een corrosiewerende stof.
- Het wordt gebruikt als een levensmiddelenadditief dat de zuurgraad reguleert in meeldeeg en brood.
referenties
- OESO SIDS. (Oktober 2004). Ammoniumsulfaat. [PDF]. Opgehaald op 27 april 2018, vanaf: inchem.org
- The Mosaic Company. (2018). Ammoniumsulfaat. Opgehaald op 27 april 2018, vanaf: cropnutrition.com
- Wikipedia. (2018). Ammoniumsulfaat. Opgehaald op 27 april 2018, van: en.wikipedia.org
- PubChem. (2018). Ammoniumsulfaat. Opgehaald op 27 april 2018, vanaf: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 juli 2015). [Afbeelding]. Opgehaald op 27 april 2018, vanaf: flickr.com
- Paula Papp (22 februari 2017). Toepassingen en toepassingen van ammoniumsulfaat. Opgehaald op 27 april 2018, vanaf: business.com


