Proteinase K-kenmerken, enzymatische activiteit en toepassingen
de proteinase K is een enzym dat behoort tot de groep van serineproteasen, dat wil zeggen, het heeft in zijn actieve katalytische centrum een aminozuurserine en heeft de functie van het verbreken van de peptidebindingen door hydrolyse. Op zijn beurt behoort dit enzym tot de familie van eiwitten subtilisins (peptidase S8).
Proteinase K heeft een molecuulgewicht (MW) van 28.900 dalton en werd voor het eerst in 1974 geïsoleerd uit extracten van de schimmel Engyodontium album, eerder bekend onder de naam Tritirachium album Limber.
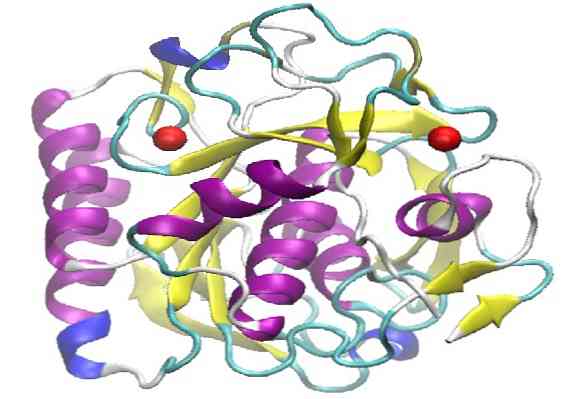
Het vertoont een hoog proteolytisch vermogen, waarvan is aangetoond dat het in staat is om de in het haar aanwezige keratine af te breken. Het woord keratine in het Engels is "keratine" geschreven, vandaar dat het "proteinase K" is.
Vanwege zijn hoge capaciteit om inheemse eiwitten te splitsen, is dit enzym bruikbaar in verschillende moleculaire biologische technieken. Het wordt voornamelijk gebruikt voor het isoleren en bereiden van nucleïnezuren met hoog moleculair gewicht (MW).
Proteinase K werkt door het nucleaire DNA vrij te maken, terwijl het de eiwitten vernietigt en de RNasen en DNasen inactiveert, dat wil zeggen, de nucleasen in de DNA- en RNA-preparaten elimineert..
Aan de andere kant is gezien dat proteinase K enkele gedenatureerde natieve eiwitten kan hydrolyseren, wat de interesse van onderzoekers heeft gewekt voor het gebruik ervan in de studie van prioneiwitten (PrPC).
Ondanks zijn hoge potentie aanwezig proteolytische eiwitten die resistent zijn tegen de werking van proteïnase K. Onder hen, wat abnormale eiwitten genaamd prionen (PrPSc) zijn geassocieerd met TSE zijn.
index
- 1 Kenmerken van proteinase K
- 2 Enzymatische activiteit
- 3 toepassingen
- 4 Voordelen van proteinase K
- 5 Proteinase-resistente eiwitten K
- 6 Referenties
Kenmerken van proteinase K
Proteinase K heeft een tertiaire structuur gevormd door drie lagen, met een β-vel van zeven ketens afgewisseld tussen twee lagen helices. Omdat het behoort tot de familie van S8-peptidasen, wordt het gekenmerkt door het hebben van een katalytische triade in zijn actieve plaats, waarvan de volgorde achtereenvolgens (Asp, His en Ser) is, die hen van andere families van peptidasen onderscheidt..
Dit enzym uit de groep van serineproteasen wordt gekenmerkt door het hydrolyseren van de peptidebindingen dichtbij de carboxylgroep van de alifatische en aromatische aminozuren.
Bovendien kan optreden in aanwezigheid van bepaalde corrosieve, zoals natriumdodecylsulfaat (SDS), Tris-HCL en EDTA, die gebruikt worden om de denaturatie van eiwitten te helpen, waardoor ze hun originele structuur stoffen verliezen.
Dit is een voorafgaande stap in de bereiding van eiwitten voor de elektroforese-techniek. Het pH-bereik waarbij proteinase K werkt is tamelijk breed (2,0 tot 12,0), met een optimale pH tussen 7,5 en 12,0, en het isoelektrische punt ervan is 8,9. Zoals kan worden waargenomen, is het actief tegen een zeer breed pH-bereik.
Een ander kenmerk dat opvalt in proteïnase K is de stabiliteit in de aanwezigheid van hoge temperaturen (50 - 60 ° C).
Enzymatische activiteit
Proteinase K heeft de aanwezigheid van calciumion nodig, hoewel dit de activiteit niet beïnvloedt, als het essentieel is om zijn stabiliteit te behouden.
Voor de proteinase K om de volledige digestie van het substraat uit te voeren, is een geschatte contacttijd tussen 5 minuten en 2 uur noodzakelijk.
In dit verband Daza et al vergeleken de zuiverheid van het DNA verschillende belichtingstijden verkregen tegen proteïnase K en concludeerde dat langdurige incubatie (tot 24 uur) aanzienlijk verbetert de kwaliteit van het DNA.
Nu, in relatie tot de concentratie die wordt gebruikt van het proteinase K-enzym in de verschillende protocollen, kan worden gezegd dat het zeer gevarieerd is.
Het kan worden gebruikt van zeer lage concentraties (5 μg / ml) tot concentraties van 500 μg / ml. Maar de meest frequente werkconcentraties liggen tussen 50 - 100 μg / ml, vooral voor de eiwitvertering en deactivering van nuclease. Hoewel een concentratie van 2 mg / ml nodig is voor weefselbehandeling.
toepassingen
De toepassingen zijn zeer breed en kunnen als volgt worden samengevat:
-Het wordt gebruikt bij de vertering van eiwitten en DNA-extractie werkwijzen zoals verscheidene voordelen: uitzouten, PK-SDS, cetyltrimethylammoniumbromide ammoniumbromide (CTAB), en kaliumacetaat gemodificeerd extractie met natriumjodide.
-Inactivatie van nucleasen (RNases en DNases).
-In de hybridisatietechniek in situ (HIS), om het nucleïnezuur te helpen vrijmaken, naast het elimineren van ongewenste eiwitten.
-Eiwit modificatie.
-Op onderzoeksniveau, in verschillende onderzoeken.
Voordelen van proteinase K
Verschillende vergelijkende studies zijn uitgevoerd onder DNA-extractietechnieken met behulp van Proteinase K, met andere die het niet gebruiken en alle concluderen dat er meer voordelen zijn bij het gebruik van het enzym. Een van de voordelen is het volgende:
-Hoogwaardig DNA van hoge kwaliteit en zuiverheid wordt verkregen.
-Het geëxtraheerde DNA is stabiel tot 3 maanden.
Het geëxtraheerde DNA kan worden gebruikt in de volgende technieken: Southern blot, polymerasekettingreactie (PCR), elektroforese, onder andere.
Eiwitten die resistent zijn tegen proteïnase K
Onderzoek heeft geconcludeerd dat prionen (PrPSc toxische abnormale eiwitten) worden onderscheiden van PrP c eiwit (native) bestand tegen de werking van proteïnase K zijn, terwijl PrP c gevoelig voor actie.
Andere auteurs hebben beschreven dat in de structuur van PrPSc er gevoelige delen zijn en andere resistent zijn tegen proteïnase K. Beide delen zijn echter even toxisch en infectieus..
Aan de andere kant isoleerden Bastian en medewerkers in 1987 4 eiwitten van 28, 30, 66 en 76 kda van een soort Spiroplasma mirum. Alle waren resistent tegen de werking van proteinase K en hadden ook een kruisreactie met enkele prionen.
Het is bekend dat deze soort staar en aanzienlijke neurologische schade kan veroorzaken en als gevolg van wetenschappelijke bevindingen Bastian, onder andere onderzoek, heeft geprobeerd om te linken naar dit micro-organisme met overdraagbare spongiforme encefalopathieën.
De etiologie van deze degeneratieve neurologische pathologie wordt echter nog steeds toegeschreven aan prionen vandaag.
In deze zin identificeerden en karakteriseerden Butler en medewerkers in 1991 een klasse van 40 Kda proteïnase resistent proteïne K uit twee stammen van Mycoplasma hyorhinis. Dit pathogeen tast de varkens aan, infecteert hun weefsels, maar in dit geval was er geen kruisreactie met de geteste prionen.
Meer onderzoek is nodig om veel onbekenden erover op te helderen.
referenties
- Bastian F, Jennings R, en Gardner W. 1987. Antiserum tegen scrapie-geassocieerd fibril eiwit kruisreageert met Spiroplasma mirum fibril-eiwitten. J. Clin. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Evaluatie van een DNA-extractie- en zuiveringsmethode uit spierweefsel gefixeerd in formaldehyde van niet-geïdentificeerde kadavers. Med Magazine, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, M Frick, Evancho S, Stanbridge E, En McGarrity G. Identificatie en karakterisering van Proteïnase K-Resistant eiwitten in de leden van de Class mollicuten. Infection and Immunity, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et al. Vergelijking van twee protocollen voor het extraheren van DNA uit Trypanosoma cruzi gekweekt in axenisch medium. Rev. Peru. Med. Exp. Volksgezondheid 2014; 31 (2): 222-227. Beschikbaar op: scielo.org
- Jiménez G, Villalobos M, Jiménez E en Palma W. Bepaling van de effectiviteit van vijf DNA-extractieprotocollen uit paraffinemateriaal voor moleculaire studies. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


