Calciumbicarbonaatstructuur, eigenschappen, risico's en toepassingen
de calciumbicarbonaat is een anorganisch zout met chemische formule Ca (HCO)3)2. Het komt uit de natuur voort uit het calciumcarbonaat dat aanwezig is in kalksteenrotsen en mineralen zoals calciet.
Calciumbicarbonaat is beter oplosbaar in water dan calciumcarbonaat. Dit kenmerk heeft de vorming van karstsystemen in kalkstenen rotsen en in het structureren van grotten mogelijk gemaakt.

De onderaardse wateren die door de scheuren gaan, raken verzadigd in hun verplaatsing van koolstofdioxide (CO2). Deze wateren tasten de kalksteenrotsen aan die calciumcarbonaat afgeven (CaCO3) die het calciumbicarbonaat vormen, volgens de volgende reactie:
CaCO3(s) + CO2(g) + H2O (l) => Ca (HCO)3)2(Aq)
Deze reactie vindt plaats in grotten waar erg hard water vandaan komt. Calciumbicarbonaat wordt niet in de vaste toestand maar in een waterige oplossing, samen met het Ca2+, het bicarbonaat (HCO)3-) en het carbonaat-ion (CO32-).
Vervolgens, wanneer de verzadiging van het kooldioxide in het water afneemt, vindt de omgekeerde reactie plaats, dat wil zeggen de omzetting van het calciumbicarbonaat in calciumcarbonaat:
Ca (HCO)3)2(aq) => CO2 (g) + H2O (l) + CaCO3 (S)
Calciumcarbonaat is slecht oplosbaar in water, dit veroorzaakt dat de neerslag optreedt als een vaste stof. De bovenstaande reactie is erg belangrijk bij de vorming van stalactieten, stalagmieten en andere speleothemen in grotten.
Deze rotsachtige structuren worden gevormd door de waterdruppels die uit het plafond van de grotten vallen (bovenste afbeelding). De CaCO3 aanwezig in de waterdruppels wordt gekristalliseerd om de genoemde structuren te vormen.
Het feit dat calciumbicarbonaat niet in de vaste toestand wordt aangetroffen, heeft het gebruik ervan bemoeilijkt en er zijn weinig voorbeelden gevonden. Ook is het moeilijk om informatie te vinden over de toxische effecten ervan. Er is een rapport van een reeks bijwerkingen van het gebruik ervan als een behandeling om osteoporose te voorkomen.
structuur
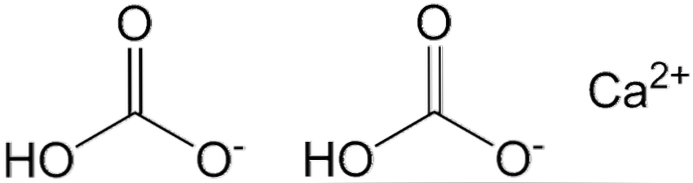
Twee HCO-anionen worden getoond in de bovenste afbeelding3- en een kation2+ interactie elektrostatisch. De Ca2+ volgens de afbeelding moet deze zich in het midden bevinden, want zo zijn de HCO's3- ze zouden elkaar niet afstoten vanwege hun negatieve beschuldigingen.
De negatieve lading in de HCO3- het is gedelokaliseerd tussen twee zuurstofatomen, door resonantie tussen de C = O-carbonylgroep en de C-O-binding-; terwijl in de CO32-, Dit is gedelocaliseerd tussen de drie zuurstofatomen, omdat de C-OH-binding gedeprotoneerd is en daarom door resonantie een negatieve lading kan ontvangen.
De geometrieën van deze ionen kunnen worden beschouwd als sferen van calcium omgeven door platte driehoeken van carbonaten met een gehydrogeneerd uiteinde. Qua maatverhouding is calcium merkbaar kleiner dan HCO-ionen3-.
Waterige oplossingen
De Ca (HCO)3)2 Het kan geen kristallijne vaste stoffen vormen en het bestaat echt uit waterige oplossingen van dit zout. In hen zijn de ionen niet alleen, zoals in het beeld, maar omgeven door H-moleculen.2O.
Hoe werken ze samen? Elk ion is omgeven door een hydratatiesfeer, die zal afhangen van het metaal, de polariteit en de structuur van de opgeloste soort.
De Ca2+ coördineert met de zuurstofatomen van water om een aquocomplex te vormen, Ca (OH)2)n2+, waarbij n in het algemeen als zes wordt beschouwd; dat is, een "waterige octaëder" rond calcium.
Terwijl HCO-anionen3- interactie met beide waterstofbruggen (OR2CO-H-OH2) of met de waterstofatomen in het water in de richting van de negatieve lading delocaliseren (HOCO)2- H-OH, dipool-ion interactie).
Deze interacties tussen de Ca2+, HCO3- en het water is zo efficiënt, dat ze het calciumbicarbonaat zeer oplosbaar maken in dat oplosmiddel; in tegenstelling tot de CaCO3, waarin de elektrostatische attracties tussen de Ca2+ en de CO32- zijn erg sterk, neerslaan uit de waterige oplossing.
Naast water zijn er CO-moleculen2 rond, die traag reageren om meer HCO te bieden3- (afhankelijk van de pH-waarden).
Hypothetische vaste stof
Tot nu toe, de groottes en ladingen van de ionen in de Ca (HCO)3)2, noch de aanwezigheid van water, leg uit waarom de vaste stof niet bestaat; dat wil zeggen, zuivere kristallen die kunnen worden gekarakteriseerd door röntgenkristallografie De Ca (HCO)3)2 is niets meer dan ionen aanwezig in het water waaruit de spelonkachtige formaties blijven groeien.
Ja Ca2+ en de HCO3- ze kunnen geïsoleerd worden van het water en de volgende chemische reactie vermijden:
Ca (HCO)3)2(aq) → CaCO3(s) + CO2(g) + H2O (l)
Vervolgens konden deze worden gegroepeerd in een witte kristallijne vaste stof met stoichiometrische verhoudingen van 2: 1 (2HCO3/ 1Ca). Er zijn geen studies over de structuur ervan, maar het kan worden vergeleken met de NaHCO3 (voor magnesiumbicarbonaat, Mg (HCO)3)2, geen van beide bestaat als solide), of met de CaCO3.
Stabiliteit: NaHCO3 vs Ca (HCO)3)2
De NaHCO3 kristalliseert in het monokliene systeem en de CaCO3 in de trigonale (calciet) en orthorhombische (aragonite) systemen. Als de Na is vervangen+ voor de Ca2+, het kristallijne netwerk zou worden gedestabiliseerd door het grotere verschil in afmetingen; dat is de Na+ omdat het kleiner is, vormt het een stabieler kristal met de HCO3- vergeleken met de Ca2+.
In feite is de Ca (HCO)3)2(aq) heeft het water nodig om te verdampen, zodat zijn ionen in een kristal kunnen worden gegroepeerd; maar het kristalrooster van deze is niet sterk genoeg om het op kamertemperatuur te doen. Wanneer het water wordt verwarmd, vindt de ontledingsreactie plaats (vergelijking hierboven).
Het Na-ion zijn+ in oplossing zou dit het kristal vormen met de HCO3- vóór zijn thermische ontbinding.
De reden waarom dan Ca (HCO)3)2 het kristalliseert (theoretisch) niet, het is door het verschil van de ionische stralen of grootten van zijn ionen, die geen stabiel kristal kunnen vormen voor de ontbinding ervan.
Ca (HCO)3)2 vs CaCO3
Als aan de andere kant, H is toegevoegd+ naar de kristallijne structuren van CaCO3, ze zouden hun fysieke eigenschappen drastisch veranderen. Misschien nemen de smeltpunten ervan aanzienlijk af en zelfs de morfologie van de kristallen verandert uiteindelijk.
Zou het de moeite waard zijn om de synthese van Ca (HCO) te proberen?3)2 Solid? Moeilijkheden kunnen de verwachtingen overschrijden, en een zout met lage structurele stabiliteit levert mogelijk geen significante extra voordelen op in toepassingen waarbij andere zouten al worden gebruikt.
Fysische en chemische eigenschappen
Chemische formule
Ca (HCO)3)2
Moleculair gewicht
162,11 g / mol
Fysieke toestand
Het verschijnt niet in vaste toestand. Het wordt gevonden in een waterige oplossing en pogingen om het om te zetten in vaste stof door verdamping van water, hebben niet gewerkt omdat het is omgezet in calciumcarbonaat.
Oplosbaarheid in water
16,1 g / 100 ml bij 0 ° C; 16,6 g / 100 ml bij 20 ° C en 18,4 g / 100 ml bij 100 ° C. Deze waarden zijn indicatief voor een hoge affiniteit van watermoleculen voor Ca-ionen (HCO)3)2, zoals uitgelegd in de vorige paragraaf. Ondertussen slechts 15 mg CaCO3 ze lossen op in een liter water, wat hun sterke elektrostatische interacties weerspiegelt.
Omdat de Ca (HCO)3)2 het kan geen vaste stof vormen, de oplosbaarheid ervan kan niet experimenteel worden bepaald. Echter, gezien de voorwaarden gecreëerd door de CO2 opgelost in het water rond de kalksteen, kon de massa calcium opgelost bij een temperatuur T worden berekend; massa, die gelijk is aan de Ca-concentratie (HCO)3)2.
Bij verschillende temperaturen neemt de opgeloste massa toe zoals getoond door de waarden bij 0, 20 en 100 ° C. Dus, volgens deze experimenten, hoeveel van de Ca (HCO) wordt bepaald3)2 lost op in de buurt van de CaCO3 in een waterig medium vergast met CO2. Zodra de CO ontsnapt2 gasvormig, de CaCO3 zal precipiteren, maar niet de Ca (HCO3)2.
Fusie en kookpunten
Het kristallijne netwerk van Ca (HCO)3)2 is veel zwakker dan de CaCO3. Als het in een vaste toestand kan worden verkregen, en de temperatuur meten waarbij het in een fusiometer smelt, zou het zeker een waarde krijgen die ver beneden 899 ° C ligt. Op dezelfde manier kan hetzelfde worden verwacht bij de bepaling van het kookpunt.
Verbrandingspunt
Het is niet brandbaar.
risico's
Aangezien deze verbinding niet bestaat in vaste vorm, is het onwaarschijnlijk dat dit een risico zou vormen om zijn waterige oplossingen te manipuleren, aangezien zowel de Ca2+ als HCO3- ze zijn niet schadelijk bij lage concentraties; en daarom zou het grootste risico dat dergelijke oplossingen zouden kunnen innemen, alleen te wijten kunnen zijn aan een gevaarlijke dosis ingenomen calcium.
Als de verbinding een vaste stof vormt, ook al kan deze fysiek verschillen van de CaCO3, de toxische effecten mogen niet verder gaan dan eenvoudig ongemak en resecties na lichamelijk contact of inademing.
toepassingen
-Calciumbicarbonaatoplossingen worden al lange tijd gebruikt om oude papieren te wassen, in het bijzonder kunstwerken of historisch belangrijke documenten.
-Het gebruik van bicarbonaatoplossingen is nuttig, niet alleen omdat ze de zuren in het papier neutraliseren, maar ook een alkalische reserve aan calciumcarbonaat verschaffen. Deze laatste compound biedt bescherming voor toekomstige schade op papier.
-Net als andere bicarbonaten, wordt het gebruikt in chemische gisten en in de formuleringen van bruistabletten of -poeders. Bovendien wordt calciumbicarbonaat gebruikt als een levensmiddelenadditief (waterige oplossingen van dit zout).
-De bicarbonaatoplossingen zijn gebruikt bij het voorkomen van osteoporose. In één geval zijn echter secundaire effecten waargenomen, zoals hypercalciëmie, metabole alkalose en nierfalen..
-Calciumbicarbonaat wordt af en toe intraveneus toegediend om het depressieve effect van hypokaliëmie op de hartfunctie te corrigeren.
-En ten slotte zorgt het voor calcium in het lichaam, dat een bemiddelaar is van spiercontractie, en tegelijkertijd de acidose corrigeert die kan optreden in een toestand van hypokaliëmie..
referenties
- Wikipedia. (2018). Calciumbicarbonaat. Genomen uit: en.wikipedia.org
- Sirah Dubois. (3 oktober 2017). Wat is calciumbicarbonaat? Opgehaald van: livestrong.com
- Science Learning Hub. (2018). Carbonaat chemie. Teruggeplaatst van: sciencelearn.org.nz
- PubChem. (2018). Calciumbicarbonaat. Teruggeplaatst van: pubchem.ncbi.nlm.nih.gov
- Amy E. Gerbracht & Irene Brückle. (1997). Het gebruik van oplossingen van calciumbicarbonaat en magnesiumbicarbonaat in workshops voor kleinschalig behoud: enquêteresultaten. Teruggeplaatst van: cool.conservation-us.org


