Tin Chloride (SnCl2) Eigenschappen, Structuur, Toepassingen en Risico's
de tinchloride (II) of stannochloride, met de chemische formule SnCl2, is een witte kristallijne vaste stof, het product van de reactie van tin en een geconcentreerde oplossing van zoutzuur: Sn (s) + 2HCl (conc) => SnCl2(aq) + H2(G). Het proces van de synthese (bereiding) bestaat uit het toevoegen van stukjes tinnen vijlsel om te reageren met het zuur.
Na het toevoegen van de stukjes tin gaat het voort met het uitvoeren van een dehydratatie en kristallisatie totdat het anorganische zout is verkregen. In deze verbinding heeft tin twee elektronen verloren uit zijn valentieschil om verbindingen met chlooratomen te vormen.
Dit kan beter worden begrepen als men de valentieconfiguratie van tin (5s25pX2pen0pz0), waarvan het paar elektronen de orbitale p bezettenX wordt gegeven aan protonen H+, om een diatomisch molecuul van waterstof te vormen. Dat wil zeggen, dit is een redox-achtige reactie.
index
- 1 Fysische en chemische eigenschappen
- 1.1 Valencia-configuratie
- 1.2 Reactiviteit
- 1.3 Reductieve activiteit
- 2 Chemische structuur
- 3 Gebruik
- 4 Risico's
- 5 Referenties
Fysische en chemische eigenschappen
De SnCl-koppelingen2 Zijn ze ionisch of covalent? De fysische eigenschappen van tin (II) chloride sluiten de eerste optie uit. De smelt- en kookpunten voor deze verbinding zijn 247 ° C en 623 ° C, een aanwijzing voor zwakke intermoleculaire interacties, een bekend feit voor covalente verbindingen.
De kristallen zijn wit, wat zich vertaalt in nulabsorptie in het zichtbare spectrum.
Valencia configuratie
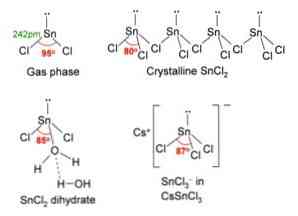
In de afbeelding hierboven, in de linkerbovenhoek, is een geïsoleerd SnCl-molecuul geïllustreerd2.
De moleculaire geometrie zou plat moeten zijn omdat de hybridisatie van het centrale atoom sp2 (3 orbitale sp2 en zuiver orbitaal om covalente bindingen te vormen), maar de vrij elektronenpaar volume inneemt en duwt de chlooratomen beneden, waardoor het molecuul een hoekige geometrie.
In gasfase wordt deze verbinding geïsoleerd, dus het heeft geen interactie met de andere moleculen.
Als een verlies van het paar elektronen in de orbitale pX, het blik wordt omgezet in het ion Sn2+ en de resulterende elektronische configuratie is 5s25pX0pen0pz0, met al zijn p orbitalen beschikbaar om links van andere soorten te accepteren.
Cl-ionen- coördineren met de Sn ion2+ om tinchloride te geven. De elektronische configuratie van tin in dit zout is 5s25pX2pen2pz0, in staat zijn om een ander paar elektronen in zijn vrije orbitale p te accepterenz.
U kunt bijvoorbeeld een andere Cl-ion accepteren-, het vormen van het complex van trigonale vlakgeometrie (een piramide met driehoekige basis) en negatief geladen [SnCl3]-.
reactiviteit
De SnCl2 heeft een hoge reactiviteit en de neiging zich te gedragen als Lewis-zuur (elektronenreceptor) om zijn valentie-octet te voltooien.
Net zoals het een Cl ion accepteert-, heeft het water, waarbij de tin gebonden aan een watermolecuul direct tin "bevochtigt" en een tweede watermolecuul vorm waterstofbinding interacties met de eerste.
Het resultaat hiervan is dat de SnCl2 het is niet zuiver, maar gecoördineerd met het water in zijn gedehydrateerde zout: SnCl2· 2H2O.
De SnCl2 Het is zeer oplosbaar in water en in polaire oplosmiddelen, omdat het een polaire verbinding is. Echter, de oplosbaarheid in water minder dan het stortgewicht mogelijk een hydrolysereactie (afbraak van een watermolecuul) een basis onoplosbaar zout genereren:
SnCl2(aq) + H2O (l) <=> Sn (OH) Cl (s) + HCl (aq)
De dubbele pijl geeft aan dat een evenwicht tot stand is gebracht, links voorkeur (richting de reagentia) als de HCl-concentraties toenemen. Hiervoor de SnCl-oplossingen2 gebruikt hebben een zure pH, om precipitatie van ongewenst zoutproduct van hydrolyse te voorkomen.
Reductieve activiteit
Reageert met zuurstof in de lucht om tin (IV) chloride of stannichloride te vormen:
6 SnCl2(aq) + O2(g) + 2H2O (l) => 2SnCl4(aq) + 4Sn (OH) Cl (s)
In deze reactie oxideert tin het vormen van een binding met het elektronegatieve zuurstofatoom en verhoogt het zijn aantal bindingen met de chlooratomen.
Over het algemeen stabiliseren de electronegatieve atomen van de halogenen (F, Cl, Br en I) de bindingen van de Sn (IV) -verbindingen en dit feit verklaart waarom de SnCl2 het is een reductiemiddel.
Wanneer het oxideert en al zijn valentie-elektronen verliest, is het Sn ion4+ het blijft met een 5s-configuratie05pX0pen0pz0, zijnde het paar elektronen in de orbitaal 5s het moeilijkst om "weggerukt" te worden.
Chemische structuur
De SnCl2 presenteert een kristalstructuur van orthorhombisch type, vergelijkbaar met rijen zagen, waarbij de uiteinden van de tanden chloriden zijn.
Elke rij is een SnCl-ketting3 een Cl-brug vormen met een ander Sn-atoom (Cl-Sn (Cl)2-Cl- ···), zoals te zien is in de bovenstaande afbeelding. Twee ketens, verbonden door zwakke interacties van het Sn-Cl-type, vormen één laag van de rangschikking, die op een andere laag wordt gelegd, enzovoort, totdat de kristallijne vaste stof is gedefinieerd.
Het vrije elektronen paar 5s2 veroorzaakt vervorming in de structuur omdat het volume inneemt (het volume van de elektronische wolk).
De Sn kan een coördinatiegetal gelijk aan negen, wat overeenkomt negen buren, het tekenen van een trigonale prisma deze zich in het midden van de geometrische figuur en Cl op de hoekpunten, en andere Cl in elke van de vierkante zijden van het prisma.
Dit wordt het gemakkelijkst waargenomen bij het overwegen van een proces waar Sn (donkergrijze gebieden) naar boven gericht, en de drie Cl verband met deze driehoeksvorm de vloer, terwijl de bovenste drie Cl vormen het driehoekige dak.
toepassingen
In organische synthese wordt het gebruikt als een reductiemiddel voor aromatische nitroverbindingen (Ar-NO2 à Ar-NH2). Omdat de chemische structuur laminair is, vindt het gebruik in de wereld van de katalyse van organische reacties, naast dat het een potentiële kandidaat is voor katalytische ondersteuning.
Het reducerende vermogen wordt gebruikt om de aanwezigheid van goudverbindingen te bepalen, om glazen te bekleden met zilveren spiegels en om als een antioxidant te fungeren.
Ook in zijn moleculaire geometrie trigonale piramide (: SnX3- M+) wordt gebruikt als Lewis-base voor de synthese van een groot aantal verbindingen (zoals het Pt-clustercomplex)3sn8cl20, waarbij het elektronenvrije paar is gecoördineerd met een Lewis-zuur).
risico's
De SnCl2 Het kan witte bloedcellen beschadigen. Het is bijtend, irriterend, carcinogeen en heeft grote negatieve gevolgen voor de soorten die in mariene ecosystemen leven.
Het kan ontleden bij hoge temperaturen, waardoor het schadelijke chloorgas vrijkomt. In contact met sterk oxiderende middelen veroorzaakt dit explosieve reacties.
referenties
- Shiver & Atkins. (2008). Anorganische chemie in De elementen van groep 14 (vierde editie., pagina 329). Mc Graw Hill.
- ChemicalBook. (2017). Opgehaald op 21 maart 2018, via ChemicalBook: chemicalbook.com
- PubChem. (2018). Tin Chloride. Opgehaald op 21 maart 2018, van PubChem: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2017). Tin (II) chloride. Opgehaald op 21 maart 2018, op Wikipedia: en.wikipedia.org
- E.G. Rochow, E.W. (1975). De chemie van Germanium: Tin en lood (eerste ed.). p-82.83. Pergamom Press.
- F. Hulliger. (1976). Structurele chemie van laag-type fases. P-120.121. D. Reidel Publishing Company.



