Natriumchloride (NaCl) -structuur, eigenschappen, toepassingen, toxiciteit
de natriumchloride, ook wel keukenzout of keukenzout genoemd, is een binair anorganisch zout van het alkalimetaal-natrium en het halogeen-chloor. Het is het grootste bestanddeel van eetbaar zout en de minerale vorm ervan staat bekend als halite. De molecuulformule ervan is NaCl en beschrijft de stoichiometrische verhouding van zijn ionen (Na+ cl-) en niet dat van een afzonderlijk molecuul (Na-Cl)
Natriumchloride is een kristallijne witte vaste stof die wordt gevormd door de combinatie van natrium, zilverachtig wit metaal, dat heftig reageert met water, en het chloorelement, een giftig, bijtend, lichtgroen gas.

In het bovenste beeld is een gedeelte van NaCl-kristallen weergegeven. Hoe is het mogelijk dat twee elementen zo gevaarlijk zijn als Na en Cl2, kan een eetbaar zout worden gevormd? Ten eerste is de chemische vergelijking voor de vorming ervan:
2Na (s) + Cl2(g) => 2NaCl (s)
Het antwoord ligt in de aard van de link in het NaCl. Ionisch zijn, de eigenschappen van Na+ en Cl- ze zijn diagonaal verschillend van die van hun neutrale atomen.
Natrium is een vitaal element, maar in zijn ionische vorm. De Na+ is het belangrijkste extracellulaire kation met een concentratie van ongeveer 140 mEq / lt, en samen met de bijbehorende anionen, de Cl- en de HCO3- (bicarbonaat), zijn voornamelijk verantwoordelijk voor de waarde van osmolariteit en extracellulair volume.
Daarnaast is de Na+ is verantwoordelijk voor het genereren en geleiden van zenuwimpulsen in neuronale axonen, evenals het initiëren van spiercontractie.
NaCl wordt al sinds de oudheid gebruikt om voedsel te smaken en vlees te bewaren, vanwege het vermogen om bacteriën te elimineren en bederf te voorkomen.
Het is ook noodzakelijk voor de productie van natriumhydroxide (NaOH) en moleculair chloor (Cl2), door het NaCl te laten reageren met het water onder hydrolyse:
2H2O (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
In de kathode (-) accumuleert de H2 (g) en NaOH. Ondertussen verzamelt de Cl zich bij de anode (+)2 (G). Natriumhydroxide wordt gebruikt bij de productie van zepen en chloor bij de vervaardiging van PVC-plastic.
index
- 1 Structuur van natriumchloride
- 1.1 Unitaire cel
- 2 Eigenschappen
- 2.1 Moleculaire formule
- 2.2 Molecuulgewicht
- 2.3 Fysieke beschrijving
- 2.4 Kleur
- 2.5 Smaak
- 2.6 Kookpunt
- 2.7 Smeltpunt
- 2.8 Oplosbaarheid in water
- 2.9 Oplosbaarheid in organische oplosmiddelen
- 2.10 Dichtheid
- 2.11 Dampspanning
- 2.12 Stabiliteit
- 2.13 Ontleding
- 2.14 Viscositeit
- 2.15 Corrosie
- 2.16 pH
- 3 Gebruik
- 3.1 In voedsel
- 3.2 Industrieel gebruik
- 3.3 Thuis
- 3.4 Andere toepassingen
- 3.5 Therapeutisch gebruik
- 4 Toxiciteit
- 4.1 Inslikken
- 4.2 Irritatie en lichamelijk contact
- 5 Referenties
Structuur van natriumchloride
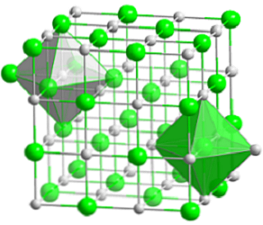
De compacte kubieke structuur van natriumchloride wordt weergegeven in het bovenste beeld. De omvangrijke groene bollen komen overeen met Cl-anionen-, terwijl wit, tegen Na-kationen+. Merk op hoe het kristal van NaCl bestaat uit een netwerk van ionen gerangschikt door hun elektrostatische interacties in een verhouding van 1: 1.
Hoewel balken in de afbeelding worden weergegeven, zijn de bindingen niet covalent maar ionisch. Het gebruik van de balken is handig wanneer de coördinatiegeometrie rond een ion wordt getoond. Bijvoorbeeld in het geval van NaCl elke Na+ is omringd door zes Cl- (witte octaëder), en elke Cl- van zes Na+ (groene octaëder).
Daarom heeft het een coördinatie (6,6) waarvan het aantal aangeeft hoeveel buren elk ion omringen. Het nummer aan de rechterkant geeft de buren van Na aan+, terwijl degene aan de linkerkant, de Cl-.
Andere afbeeldingen laten het gebruik van de balken weg om de octaëdrische gaten te markeren die de structuur heeft, die het gevolg zijn van de tussenruimte tussen zes Cl-anionen.- (of Na-kationen+) verpakt. Deze opstelling wordt waargenomen in andere mono (MX) of meeratomische anorganische zouten en wordt gem-zout genoemd..
Unitaire cel
De eenheidscel van het steenzout is kubisch, maar welke kubussen vertegenwoordigen het precies in de bovenstaande afbeelding? De octaëders geven het antwoord. Beiden bedekken in totaal vier kleine blokjes.
Deze kubussen hebben delen van de ionen in hun hoekpunten, randen en vlakken. Nauwlettend te observeren, een ion Na+ het bevindt zich in het midden en twaalf daarvan in de randen. Een ion op een rand kan worden gedeeld door vier kubussen. Dus er zijn 4 Na-ionen+ (12 × 1/4 + 1 = 4).
Voor Cl-ionen-, acht bevinden zich in de hoekpunten en zes in de randen. Omdat de ionen die op de hoekpunten zijn geplaatst, ruimte delen met acht andere kubussen en aan de randen met zes hebben ze 4 Cl-ionen- (8 × 1/8 + 6 × 1/2 = 4).
Het vorige resultaat wordt als volgt geïnterpreteerd: in de eenheidscel van NaCl zijn er vier Na-kationen+ en vier Cl-anionen-; aandeel dat overeenkomt met de chemische formule (een Na+ voor elke Cl-).
eigenschappen
Moleculaire formule
NaCl.
Moleculair gewicht
58,44 g / mol.
Fysieke beschrijving
Een kristallijne vaste stof.
kleur
Transparante kleurloze kristallen of wit kristallijn poeder.
smaak
zout.
Kookpunt
2,575 ºF tot 760 mmHg.
1.465 ºC.
Smeltpunt
1474 ºF (800,7 ºC).
Zowel het kookpunt als het smeltpunt weerspiegelen de warmte die nodig is om de kristallijne reticulaire energie te overwinnen. Daarom bevestigen deze metingen het ionische karakter van NaCl.
Oplosbaarheid in water
Groter dan of gelijk aan 100 mg / ml bij 68 ° F.
36,0 g / 100 ml bij 25 ºC.
Het is in feite een hygroscopisch zout, dat vocht uit de omgeving tegenhoudt.
Oplosbaarheid in organische oplosmiddelen
0,065 g / 100 ml ethanol bij 25 ° C; 10 g / 100 g glycerol bij 25 ° C; 2,15 g / 100 ml vloeibaar ammonium bij 40 ° C; 1,4 g / 100 ml methanol bij 25 ° C; 7,15 g / 100 ethyleenglycol bij 25 ° C en 5,21 g / 100 g mierenzuur bij 25 ° C.
dichtheid
2,165 g / cm3 bij 77 ºC.
Stoom druk
1 mmHg tot 1,589 ºF.
stabiliteit
Het is stabiel onder de aanbevolen bewaarcondities.
ontleding
Bij verhitting tot hoge temperaturen ontleedt het de uitstromende dampen van zoutzuur en dinatriumoxide.
viscositeit
Viscositeit van verzadigde oplossingen 1,93 mPa-s.
corrosie
Het is bijtend voor veel metalen.
pH
6.7 tot 7.3 in waterige oplossing.
toepassingen
In voedsel
-Natriumchloride wordt al sinds de oudheid gebruikt om de smaak van voedsel en de conservering ervan te verbeteren. Het zouten van het vlees is een manier om het tegen bacteriële actie te beschermen, omdat het de ontleding van het eiwit vertraagt.
-Aan de andere kant verhoogt het zout de osmolariteit rond het vlees, waardoor de absorptie door osmose van het water van de bacterie de eliminatie ervan veroorzaakt.
Industrieel gebruik
Voedingsindustrie
-In de voedingsindustrie wordt zout gebruikt als smaakversterker, additief voor fermentatiecontrole, textuurcontrolemiddel en kleurontwikkelaar. Er wordt bijvoorbeeld zout toegevoegd om de kleur in spek, ham en andere vleesproducten te markeren.
-Zout dient als een bindmiddel bij de vervaardiging van worsten. Het draagt bij aan de vorming van een bindmiddelgel samengesteld uit vlees, vet en vocht.
-Bij de verwerking van bloem voor het maken van brood, wordt zout toegevoegd tijdens het koken om de snelheid van fermentatie van brooddeeg te regelen. Het wordt ook gebruikt om gluten en als smaakversterker te versterken, evenals een vulling van gebakken goederen.
-Het wordt gebruikt bij de vervaardiging van ontbijtgranen, gemengde of bereide meelsoorten, frieten, maaltijden voor honden en katten, enz..
Synthese van chemische producten
-Natriumchloride wordt gebruikt als grondstof bij de productie van natriumhydroxide en chloor, wat op zijn beurt bruikbaar is in veel chemische industrieën.
-Zout wordt gebruikt bij de verwerking van verschillende metalen, bijvoorbeeld aluminium, koper, staal en vanadium. Het wordt ook gebruikt om natriumchloraat te maken, dat vervolgens wordt gebruikt bij de synthese van chloordioxide, een bleekmiddel op basis van zuurstof. Chloordioxide is minder schadelijk voor het milieu dan andere bleekmiddelen.
In de leerindustrie
-Zout wordt gebruikt om de bacteriële werking in de huid te remmen, en om te helpen bij rehydratatie.
In de textielindustrie
-Zout wordt gebruikt als bijtmiddel bij het verven van stoffen. Het wordt gebruikt als pekelspoeling om organische verontreinigingen te verwijderen en om een positieve lading op het oppervlak van de stoffen te creëren die de vereniging van de negatief geladen kleurstoffen mogelijk maakt.
In de olie-industrie
-Bij olie- en gasexploratie is zout een belangrijk onderdeel van boorvloeistoffen. Het wordt gebruikt voor het uitvlokken en vergroten van de dichtheid van boorvloeistoffen, waardoor de hoge drukken van het gas in de te bereiken putten kunnen worden overwonnen. Bovendien handhaaft het zout de verzadiging van de boorvloeistof.
-Het zout helpt om de grond waarop de wegen zijn gebouwd te verdichten. Verlaagt de verplaatsing die in de ondergrond wordt veroorzaakt door veranderingen in luchtvochtigheid en autoverkeer.
Thuis
Het zout is gebruikt door te wrijven bij het reinigen van oppervlakken, potten en pannen. Ook bij het voorkomen van schimmel en als vlekverwijderaar. Ook wordt het gebruikt in veel merken shampoo en tandpasta.
Andere toepassingen
Op de wegen
-In afwachting van sneeuwval zijn wegen bedekt met pekel, wat de vereniging van ijs aan de oppervlakte van de weg voorkomt. Voor ontdooien wordt een mengsel van pekel en zout gebruikt en soms worden andere chemische componenten zoals magnesium- of calciumchloriden toegevoegd. Het gebruik van zout en pekel is niet effectief bij temperaturen onder -10ºC.
Bij het toevoegen van zout is er een afname van het cryoscopische punt, een colligatieve eigenschap van de oplossingen, die op de een of andere manier de vorming van ijs belemmert..
-Vanwege zijn hygroscopische conditie wordt het zout gebruikt als een goedkoop droogmiddel.
In de harsen die worden gebruikt voor waterverzachting
Hard water bevat calcium- en magnesiumionen die de werking van zeep hinderen en afzettingen van basische materialen in verschillende apparatuur en leidingen produceren. Bij waterverzachting worden ionenuitwisselingsharsen gebruikt. Zout wordt gebruikt bij de bereiding en regeneratie van harsen.
Op brandblussers
Natriumchloride wordt gebruikt in brandblussers om branden te bestrijden waarin brandbare metalen aanwezig zijn, zoals magnesium, kalium, natrium en NK-legeringen.
Het zout fungeert als een koellichaam en ook als een breker die de toegang van zuurstof tot vuur beperkt.
In de bril
Natriumchloridekristallen worden gebruikt in optische componenten zoals ramen en prisma's, vooral voor infraroodlicht. Omdat het zout echter erg hygroscopisch is, treedt er een soort rijp op die de lenzen bedekt. Om deze reden zijn natriumchloride lenzen vervangen door die van zinkselenide (ZnSe).
Therapeutisch gebruik
Om het gebrek aan zouten in het lichaam aan te vullen
-Wanneer er een lichaamsuitputting van Na is+, moet worden vervangen om extracellulaire osmolariteit, zenuwgeleiding en spiercontractie te behouden.
-NaCl wordt gebruikt bij de behandeling en preventie van een tekort aan natrium en chloor, als gevolg van overmatig zweten tijdens blootstelling aan hoge temperaturen. Het wordt ook gebruikt bij excessieve diurese of overmatige beperking van zoutinname.
-Parenterale toediening van een 045% NaCl-oplossing wordt gebruikt bij de behandeling van hyperosmolaire diabetes. Het vervult een rehydraterende functie en dient om de status van de nierfunctie te evalueren.
-Injecties van hypertonische oplossingen, met een NaCl-concentratie van meer dan 0,9% g / v,
-Ze worden gebruikt als er een ernstige uitputting van Na is+, zijnde een herstel van het essentiële ion. Deze hyponatriëmie kan het gevolg zijn van een behandeling met vrije elektrolyten of met een concentratie van Na+.
Hyponatriëmie kan ook worden veroorzaakt door overmatige waterinname, niet onder controle door een ontoereikende nierfunctie.
In behandelingen en onconventioneel gebruik
-NaCl-inhalatieoplossingen worden gebruikt om de geneesmiddelen die tijdens het vernevelingsproces worden gebruikt, te verdunnen. Het wordt ook gebruikt voor tracheale was en irrigatie. 0,9% zoutoplossing gebruikt in neussprays.
-20% NaCl-oplossingen worden gebruikt voor intra-amniotische transabdominale installatie, waardoor een late abortus wordt geïnduceerd tijdens het tweede trimester van de zwangerschap.
-Natriumchloride kan als lokaal antisepticum worden gebruikt. Dankzij zijn osmotische capaciteit is het in staat om een breed spectrum van virussen en bacteriën in een onverbrande staat te dehydrateren; daarom wordt het gebruikt als een pijnlijk antisepticum om wonden te desinfecteren.
toxiciteit
inname
Het heeft alleen een schadelijk effect op de gezondheid als de inname hoog is en voor een lange tijd. Onder deze omstandigheden zou hypernatriëmie optreden met als gevolg een toename in extracellulair volume dat zou leiden tot hoge bloeddruk.
Irritatie en lichamelijk contact
Het heeft alleen een toxisch effect als de inhalatie erg hoog is. Bij overmatig contact met de huid kan de huid droog worden. Ten slotte veroorzaakt het een tijdelijke irritatie bij contact met de ogen.
referenties
- Shiver & Atkins. (2008). Anorganische chemie (Vierde editie, pagina's 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Chemie. (8e druk). CENGAGE Leren, p 482-483.
- Natriumchloride (2018). Natriumchloride: voordelen, gebruik, eigenschappen, risico's. Genomen uit: clorurodesodio.org
- PubChem. (2018). Natriumchloride. Teruggeplaatst van: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Natriumchloride. Genomen uit: en.wikipedia.org
- Amerikaanse elementen. (2018). Natriumchloride. Genomen uit: americanelements.com


