Verschillen tussen organische en anorganische verbindingen
de belangrijkste verschil tussen organische en anorganische verbindingen is de aanwezigheid van een koolstofatoom.
Organische verbindingen bevatten een koolstofatoom en hebben meestal ook een waterstofatoom om koolwaterstoffen te vormen. Van zijn kant bevat bijna geen van de anorganische verbindingen koolstof- en / of waterstofatomen.
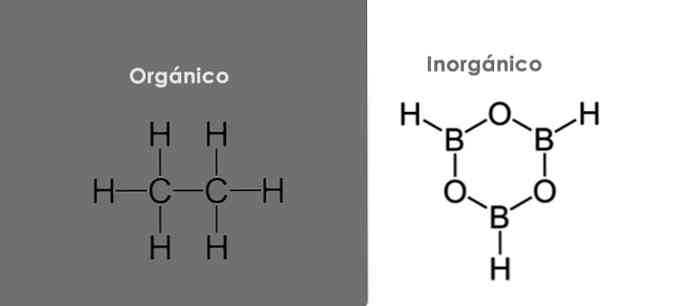
Belangrijkste verschillen tussen organische en anorganische verbindingen
Hoewel de overgrote meerderheid van anorganische verbindingen geen koolstof bevatten, zijn er enkele uitzonderingen. Koolmonoxide en koolstofdioxide bevatten bijvoorbeeld koolstofatomen.
De hoeveelheid is echter niet voldoende om sterke bindingen te vormen met de zuurstof die in het molecuul aanwezig is. Daarom hebben wetenschappers deze verbindingen altijd als anorganisch beschouwd. Daarom, zelfs als een verbinding steenkool bevat, wordt het niet noodzakelijk als organisch beschouwd.
Een ander groot verschil tussen beide verbindingen is het type molecuul en de associatie met levende wezens. Organische verbindingen omvatten zaken als de nucleïnezuren die worden gevonden in DNA, lipiden, suikers, lipidenzuren die worden aangetroffen in de cellen van levende organismen, eiwitten en enzymen die nodig zijn om celprocessen te laten plaatsvinden. Koolwaterstofbrandstoffen worden ook als organisch beschouwd.
Anorganische verbindingen van hun kant omvatten elementen zoals zouten, metalen en andere essentiële componenten. Stoffen gemaakt van solitaire elementen en elke verbinding die geen koolstofatomen heeft gebonden aan waterstofatomen, worden ook als anorganisch beschouwd.
Ondanks deze kenmerken hebben organische chemici geen definitieve overeenkomst bereikt tussen het verschil tussen organische en anorganische verbindingen. Omdat ze nog steeds een debat vormen, verwijzen ze naar de aanwezigheid van koolstof in het molecuul als de meest geaccepteerde identificatiemethode.
Organische verbindingen
In deze verbindingen zijn één of meer koolstofatomen gehecht aan atomen van andere elementen. De meest voorkomende elementen waaraan ze gehecht zijn, zijn meestal waterstof, zuurstof en stikstof. De weinige verbindingen die koolstof bevatten en niet als organisch worden beschouwd, zijn cyaniden, carbonaten en carbiden..
Traditioneel beschouwd als organische verbindingen van groot belang, omdat alle bekende leven is gebaseerd op organische verbindingen. De meest basale petrochemicaliën worden beschouwd als de basis van de organische chemie.
De moderne definitie van een organische verbinding is elke verbinding die een aanzienlijke hoeveelheid koolstof bevat, hoewel veel van de organische verbindingen die vandaag de dag bekend zijn geen verband houden met een stof die voorkomt in levende organismen.
Er zijn verschillende verbindingen die als organisch worden beschouwd, hoewel ze geen waterstof- en koolstofbindingen hebben. Deze omvatten benzeenexol, mesoxaalzuur en koolstoftetrachloride.
Organische verbindingen kunnen worden ingedeeld in natuurlijke verbindingen en synthetische verbindingen.
Natuurlijke verbindingen
Ze verwijzen naar die verbindingen geproduceerd door planten en door dieren. Veel van deze verbindingen worden gewonnen uit natuurlijke bronnen omdat het erg duur zou zijn om ze kunstmatig te produceren.
De meest voorkomende zijn suikers, sommige alkaloïden en voedingsstoffen zoals vitamine B12. Over het algemeen zijn het allemaal verbindingen die grote of gecompliceerde moleculen hebben en die in redelijke hoeveelheden in levende organismen te vinden zijn.
Synthetische verbindingen
De verbindingen die worden bereid door de reactie van andere verbindingen worden beschouwd als synthetisch. Het kunnen verbindingen zijn die in de natuur worden aangetroffen of verbindingen die niet van nature voorkomen.
De meeste polymeren, zoals kunststoffen en rubber, zijn semi-synthetische organische verbindingen.
biotechnologie
Veel organische verbindingen, zoals ethanol en insuline, worden industrieel vervaardigd met behulp van organismen uit bacteriën en gist. Typisch wordt het DNA van een organisme veranderd om verbindingen tot expressie te brengen die normaal niet in het lichaam worden geproduceerd.
Veel verbindingen gemaakt door biotechnologie bestonden eerder niet in de natuur.
Anorganische verbindingen
Een verbinding kan als anorganisch worden beschouwd als deze geen binding tussen koolstof en waterstof bevat, de C-H-lus in de chemie, in de samenstelling ervan. Bovendien zijn anorganische verbindingen meestal op mineralen gebaseerde mineralen of verbindingen die geen koolstof bevatten dat aan waterstofmoleculen is gebonden. Dit is de reden waarom veel van de anorganische verbindingen metalen zijn.
Er kan worden gezegd dat een verbinding als anorganisch wordt beschouwd als deze aan een van deze criteria voldoet:
- Er is geen aanwezigheid van steenkool in zijn samenstelling.
- Het is van niet-biologische oorsprong.
- Het kan niet worden gevonden of opgenomen in een levend organisme.
Op dit moment kunnen anorganische verbindingen ook worden gedefinieerd als elke verbinding die niet van organische aard is.
Het is om deze reden dat sommige eenvoudige verbindingen die koolstof bevatten, anorganisch worden genoemd. Sommige van deze verbindingen omvatten koolmonoxide, koolstofdioxide, natriumbicarbonaat, carbiden, carbonaten en cyaniden..
Veel van deze verbindingen zijn normale delen van veel meestal organische systemen, inclusief organismen. Dit betekent dat een chemische stof als anorganisch kan worden beschreven, maar dit betekent niet dat deze niet voorkomt in levende organismen.
De mineralen zijn meestal oxiden en sulfaten, die strikt anorganisch zijn, hoewel ze van biologische oorsprong zijn. In feite is het grootste deel van planeet Aarde anorganisch.
Hoewel de componenten van de aardlagen goed zijn opgehelderd, blijven het mineralisatieproces en de samenstelling van de diepe laag als actieve gebieden in het onderzoek.
De waarheid is dat de meeste verbindingen in het universum anorganisch van aard zijn. Om deze reden hebben anorganische verbindingen een geweldige toepassing en vele praktische toepassingen in het dagelijks leven. Omdat veel van de verbindingen in de wereld anorganisch zijn, kunnen deze verbindingen veel verschillende vormen hebben en kunnen ze zeer verschillende kenmerken hebben.
Omdat veel metalen zijn, kunnen ze bijvoorbeeld elektriciteit overbrengen. Ze hebben ook de neiging om hoge kookpunten te hebben, evenals zeer levendige en heldere kleuren. Meestal lossen ze heel goed op in water en veel van hen hebben het vermogen om kristallen te vormen.
referenties
- Organische versus anorganische verbindingen. Zachte scholen. Hersteld van softschools.com.
- Wat is het verschil tussen organisch en anorganisch? (2016) Wetenschap. Opgehaald van thoughtco.com.
- Organische samenstelling. Chemische verbindingen. Encyclopedie Britannica. Hersteld van britannica.com.
- Amerikaanse brandstof- en petrochemische fabrikanten. (2016). Hersteld van afpm.org.
- Geomicrobiologie: Hoe moleculaire wetenschappelijke interacties de basis vormen voor biochemische systemen. (2002). Wetenschap -296. Opgehaald van sciencemag.org.
- Wat zijn anorganische verbindingen? Definitie, kenmerken en voorbeelden. Les 20, hoofdstuk 4. Ontvangst van study.com.


