Atoomstraal hoe het wordt gemeten, hoe het in het periodiek systeem verandert, voorbeelden
de atomaire straal het is een belangrijke parameter voor de periodieke eigenschappen van de elementen van het periodiek systeem. Het is direct gerelateerd aan de grootte van de atomen, omdat bij grotere straal groter of omvangrijker zijn. Evenzo is het gerelateerd aan de elektronische kenmerken van hetzelfde.
Zolang een atoom meer elektronen heeft, hoe groter de grootte en atomaire straal. Beide worden gedefinieerd door de elektronen van de valentie-schaal, omdat op afstanden buiten hun banen de kans op het vinden van een elektron nul nadert. Het tegenovergestelde gebeurt in de buurt van de kern: de kans op het vinden van een elektron neemt toe.

Het bovenste beeld geeft een verpakking van katoenen ballen weer. Merk op dat elk wordt omringd door zes buren, zonder een andere mogelijke bovenste of onderste rij te tellen. De manier waarop katoenen ballen worden gecomprimeerd, bepaalt hun afmetingen en dus hun stralen; net zoals het gebeurt met atomen.
Elementen volgens hun chemische aard interageren op de een of andere manier met hun eigen atomen. Daarom varieert de grootte van de atomaire straal afhankelijk van het type binding dat aanwezig is en de vaste pakking van zijn atomen.
index
- 1 Hoe wordt de atomaire straal gemeten?
- 1.1 Bepaling van de internucleaire afstand
- 1.2 eenheden
- 2 Hoe verandert dit in het periodiek systeem?
- 2.1 Over een periode
- 2.2 Afdalen door een groep
- 2.3 Lanthanidesamentrekking
- 3 voorbeelden
- 4 Referenties
Hoe wordt de atomaire radius gemeten?
In de hoofdafbeelding kan het eenvoudig zijn om de diameter van de katoenen ballen te meten en deze vervolgens door twee te delen. De bol van een atoom is echter niet volledig gedefinieerd. Waarom? Omdat elektronen circuleren en diffunderen in specifieke gebieden van de ruimte: orbitalen.
Daarom kan het atoom worden beschouwd als een bol met ongrijpbare randen, waardoor het onmogelijk is om met zekerheid te zeggen in hoeverre ze eindigen. In de bovenste afbeelding bijvoorbeeld, ziet het middengebied, bij de kern, een intensere kleur, terwijl de randen wazig zijn.
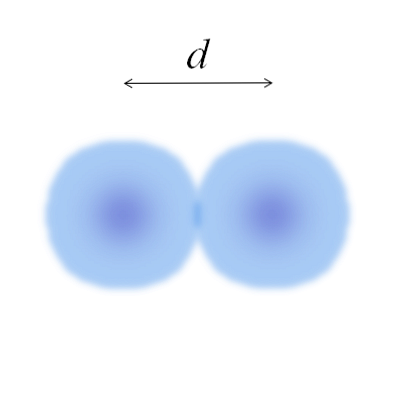
Het beeld vertegenwoordigt een diatomisch molecuul E2 (zoals de Cl2, H2, O2, etc.). Ervan uitgaande dat de atomen bolvormige lichamen zijn, als de afstand werd bepaald d die beide kernen in de covalente binding scheidt, dan zou het voldoende zijn om het in twee helften te verdelen (d/ 2) om de atomaire straal te verkrijgen; meer precies, de covalente straal van E voor E2.
En als E geen covalente binding met zichzelf vormt, maar het is een metaalachtig element? dan d het zou worden aangegeven door het aantal buren dat E omgeeft in zijn metalen structuur; dat wil zeggen, door het coördinatienummer (N.C) van het atoom in de verpakking (onthoud de katoenen bollen van het hoofdbeeld).
Bepaling van de internucleaire afstand
Om te bepalen d, wat de internucleaire afstand is voor twee atomen in een molecuul of verpakking, het vereist fysische analysetechnieken.
Een van de meest gebruikte is röntgendiffractie, daarin wordt een lichtstraal door een kristal bestraald en het diffractiepatroon als gevolg van de interacties tussen elektronen en elektromagnetische straling wordt bestudeerd. Afhankelijk van de verpakking kunnen verschillende diffractiepatronen worden verkregen en dus andere waarden van d.
Als de atomen "strak" in het kristalrooster zitten, zullen ze verschillende waarden weergeven d vergeleken met wat ze zouden hebben als ze "comfortabel" waren. Deze internucleaire afstanden kunnen ook oscilleren in waarden, dus de atomaire radius bestaat eigenlijk uit een gemiddelde waarde van dergelijke metingen.
Hoe is de atomaire straal en het coördinatiegetal gerelateerd? V. Goldschmidt vestigde een relatie tussen de twee, waarin voor een N.C van 12 de relatieve waarde 1 is; van 0,97 voor een pakking waarbij het atoom gelijk is aan N.C; van 0,96, voor een N.C gelijk aan 6; en 0,88 voor een N.C van 4.
units
Uit de waarden voor N.C gelijk aan 12, zijn veel tabellen geconstrueerd die de atomaire radii van alle elementen van het periodiek systeem vergelijken.
Omdat niet alle elementen zulke compacte structuren vormen (N.C minder dan 12), wordt de relatie van V. Goldschmidt gebruikt om hun atomaire radii te berekenen en ze uit te drukken voor dezelfde verpakking. Op deze manier zijn metingen van atomaire radii gestandaardiseerd.
Maar in welke eenheden drukken ze zichzelf uit? gezien het feit dat d is van een zeer kleine omvang, moet worden teruggevoerd naar de Angström eenheden Å (10 ∙ 10-10m) of ook op grote schaal gebruikt, de picometer (10 ∙ 10-12m).
Hoe verandert het in het periodiek systeem?
Gedurende een periode
De atoomstralen bepaald voor metalen elementen krijgen de naam van metalen stralen, terwijl voor die niet-metalen elementen, covalente stralen (zoals fosfor, P4, of de zwavel, S8). Tussen beide soorten radio's is er echter een duidelijker onderscheid dan de naam.
Van links naar rechts in dezelfde periode voegt de kern protonen en elektronen toe, maar de laatste zijn beperkt tot hetzelfde energieniveau (hoofdkwantumnummer). Als gevolg oefent de kern een toenemende effectieve nucleaire lading uit op de valentie-elektronen, die de atomaire straal samentrekt.
Op deze manier hebben niet-metalen elementen in dezelfde periode de neiging atomaire (covalente) radii kleiner te zijn dan metalen (metalen radii).
Aflopend door een groep
Bij afdalen door een groep worden nieuwe niveaus van energie mogelijk gemaakt, waardoor de elektronen meer ruimte hebben. Dus, de elektronische wolk dekt grotere afstanden af, de wazige omtrek eindigt meer weg van de kern en daarom breidt de atoomstraal zich uit.
Lanthanidesamentrekking
De elektronen van de binnenste laag helpen de effectieve nucleaire lading op de valentie-elektronen af te schermen. Wanneer de orbitalen die deel uitmaken van de binnenste lagen veel "gaten" (knooppunten) hebben, zoals bij de f-orbitalen, trekt de kern sterk de atoomstraal samen vanwege het slechte afschermeffect van de orbitalen..
Dit feit blijkt uit de lanthanidesamentrekking in periode 6 van het periodiek systeem. Van La naar Hf is er een aanzienlijke samentrekking van de atoomstraal die wordt geproduceerd door de orbitalen f, die "opvullen" als men door blok f gaat: dat van de lanthanoïden en actinoïden.
Een vergelijkbaar effect kan ook worden waargenomen met de elementen van het blok p uit periode 4. Dit tijdproduct van het zwakke afschermeffect van de orbitalen d die opvullen bij het overschrijden van de perioden van de overgangsmetalen.
Voorbeelden
Voor periode 2 van het periodiek systeem zijn de atomaire stralen van de elementen:
-Li: 257 pm
-Be: 112 pm
-B: 88 uur
-C: 77 uur
-N: 74 uur
-O: 66 uur
-F: 64 p.m.
Merk op dat lithiummetaal de grootste atomaire radius (257 p.m.) heeft, terwijl fluor, uiterst rechts van de periode, de kleinste is (64 p.m.). De atoomstraal daalt in dezelfde periode van links naar rechts en de weergegeven waarden laten dit zien.
Lithium, door het vormen van metalen bindingen, de straal is metaalachtig; en fluor, omdat het covalente bindingen (F-F) vormt, is zijn straal covalent.
En als je de atoom-radio's in eenheden van angstrom wilt uitdrukken? Deel ze eenvoudig in op 100: (257/100) = 2.57Å. En zo verder met de rest van de waarden.
referenties
- Chemistry 301. Atomic Radii. Teruggeplaatst van: ch301.cm.utexas.edu
- CK-12 Foundation. (28 juni 2016). Atomic Radius. Teruggeplaatst van: chem.libretexts.org
- Trends in atomaire radiii. Genomen uit: intro.chem.okstate.edu
- Clackamas Community College. (2002). Atoomgrootte. Teruggeplaatst van: dl.clackamas.edu
- Clark J. (augustus 2012). Atoom en Ionische straal. Teruggeplaatst van: chemguide.co.uk
- Shiver & Atkins. (2008). Anorganische chemie (Vierde editie., Blz. 23, 24, 80, 169). Mc Graw Hill.


