Ethylether eigenschappen, structuur, verkrijgen, gebruiken
de ethylether, ook bekend als diethylether, is een organische verbinding waarvan de chemische formule C is4H10O. Het wordt gekenmerkt door een kleurloze en vluchtige vloeistof, en daarom moeten de flessen zo hermetisch mogelijk worden gesloten.
Deze ether is geclassificeerd als een lid van de dialkylethers; dat wil zeggen, ze hebben de formule ROR ', waarbij R en R' verschillende koolstofsegmenten voorstellen. En zoals het zijn middelste naam, diëthylether, beschrijft, zijn twee radicalen -ethyl die binden aan het zuurstofatoom.

Aanvankelijk werd ethylether gebruikt als algemeen verdovingsmiddel, in 1846 geïntroduceerd door William Thomas Green Morton. Vanwege de ontvlambaarheid werd het gebruik echter afgewezen en vervangen door andere, minder gevaarlijke anesthetica..
Deze verbinding is ook gebruikt om de bloedingstijd te schatten, tijdens de beoordeling van de cardiovasculaire status van patiënten.
In het lichaam kan diethylether worden omgezet in koolstofdioxide en metabolieten; de laatste wordt uitgescheiden in de urine. Het meeste van de toegediende ether wordt echter uitgeademd in de longen, zonder enige modificatie te ondergaan.
Aan de andere kant wordt het gebruikt als een oplosmiddel voor zepen, oliën, parfums, alkaloïden en tandvlees.
index
- 1 Structuur van ethylether
- 1.1 Intermoleculaire krachten
- 2 Fysische en chemische eigenschappen
- 2.1 Andere namen
- 2.2 Moleculaire formule
- 2.3 Molecuulgewicht
- 2.4 Fysieke verschijning
- 2.5 Geur
- 2.6 Smaak
- 2.7 Kookpunt
- 2,8 Smeltpunt
- 2.9 Vlampunt
- 2.10 Oplosbaarheid in water
- 2.11 Oplosbaarheid in andere vloeistoffen
- 2.12 Dichtheid
- 2.13 Dampdichtheid
- 2.14 Dampspanning
- 2.15 Stabiliteit
- 2.16 Automatische ontsteking
- 2.17 Ontleding
- 2.18 Viscositeit
- 2.19 Verbrandingswarmte
- 2.20 Verdampingswarmte
- 2.21 Oppervlaktespanning
- 2.22 Ionisatiepotentieel
- 2.23 Geurdrempel
- 2.24 Brekingsindex
- 3 Verkrijgen
- 3.1 Van ethylalcohol
- 3.2 Van ethyleen
- 4 Toxiciteit
- 5 Gebruik
- 5.1 Organisch oplosmiddel
- 5.2 Algemene anesthesie
- 5.3 Geest van de ether
- 5.4 Evaluatie van de bloedsomloop
- 5.5 Onderwijslaboratoria
- 6 Referenties
Structuur van ethylether
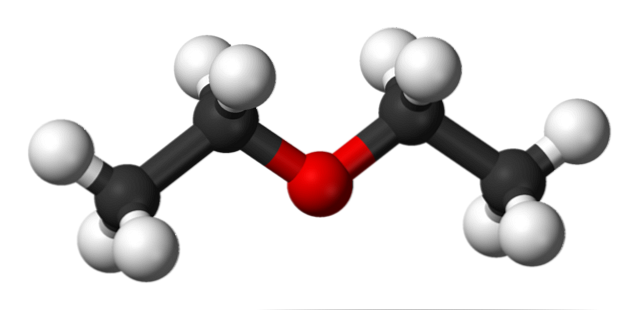
In de bovenstaande afbeelding hebben we een afbeelding met een model van bollen en staven van de moleculaire structuur van ethylether.
Zoals te zien is, heeft de rode bol, corresponderend met het zuurstofatoom, aan beide zijden twee ethylgroepen. Alle verbindingen zijn eenvoudig, flexibel en vrij draaibaar rond de assen σ.
Deze rotaties zijn afkomstig van stereoisomeren die bekend staan als conformers; dat meer dan isomeren, het zijn alternatieve ruimtelijke toestanden. De structuur van het beeld komt exact overeen met de anti-conformer, waarin alle groepen atomen verspringend zijn (gescheiden van elkaar).
Wat zou de andere conformer zijn? De verduistering, en hoewel je afbeelding niet beschikbaar is, visualiseer het dan gewoon met een U-vorm. Aan de bovenkant van de U bevinden zich de methylgroepen, -CH3, die sterische afstotingen zouden ervaren (ze zouden botsen in de ruimte).
Daarom wordt verwacht dat het CH-molecuul3CH2OCH2CH3 neem de meeste anticonceptie over.
Intermoleculaire krachten
Door welke intermoleculaire krachten worden de moleculen van ethylether gereguleerd in de vloeibare fase? Ze worden hoofdzakelijk in de vloeistof gehouden dankzij de dispersiekrachten, aangezien hun dipoolmoment (1.5D) een regio mist met een tekort aan elektronische dichtheid (δ +)
Dit komt omdat geen enkel koolstofatoom van de ethylgroepen te veel elektronendichtheid geeft aan het zuurstofatoom. Het bovenstaande is duidelijk met de kaart van elektrostatische potentiaal van ethylether bij de hand (afbeelding onderaan). Let op de afwezigheid van een blauwe regio.
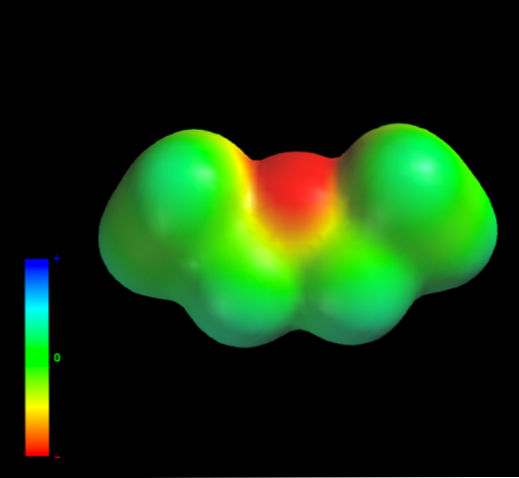
Zuurstof kan ook geen waterstofbruggen vormen, omdat er geen O-H-bindingen beschikbaar zijn in de moleculaire structuur. Daarom zijn het de ogenblikkelijke dipolen en hun moleculaire massa die hun verspreidingskrachten begunstigen.
Desondanks is het sterk oplosbaar in water. Waarom? Omdat het zuurstofatoom, met een hogere elektronendichtheid, waterstofbruggen van een watermolecuul kan accepteren:
(CH3CH2)2Oδ- - δ+H-OH
Deze interacties zijn verantwoordelijk voor 6,04 g van deze ether die oplost in 100 ml water.
Fysische en chemische eigenschappen
Andere namen
-Diethyl ether
-ethoxyethaan
-Ethyloxide
Moleculaire formule
C4H10O of (C2H5)2O.
Moleculair gewicht
74,14 g / mol.
Uiterlijke verschijning
Kleurloze vloeistof.
geur
Zoet en pittig.
smaak
Branden en zoet.
Kookpunt
94,3 ºF (34,6 ºC) tot 760 mmHg.
Smeltpunt
-177,3 ºF (-116,3 ° C). Stabiele kristallen.
Ontstekingspunt
-49ºF (gesloten container).
Oplosbaarheid in water
6,04 g / 100 ml bij 25 ° C.
Oplosbaarheid in andere vloeistoffen
Mengbaar met alifatische alcoholen met korte keten, benzeen, chloroform, petroleumether, vetoplosmiddel, veel oliën en geconcentreerd zoutzuur.
Oplosbaar in aceton en zeer oplosbaar in ethanol. Het is ook oplosbaar in nafta, benzeen en oliën.
dichtheid
0,714 mg / ml bij 68 ° F (20 ° C).
Dampdichtheid
2.55 (in relatie tot lucht genomen met dichtheid 1).
Stoom druk
442 mmHg bij 68 ° F. 538 mmHg bij 25 ° C. 58,6 kPa bij 20 ºC.
stabiliteit
Het wordt langzaam geoxideerd door de werking van lucht, vocht en licht met de vorming van peroxiden.
De vorming van peroxiden kan plaatsvinden in ethercontainers die zijn geopend en die langer dan zes maanden in opslag blijven. Peroxiden kunnen detoneren door wrijving, impact of verwarming.
Contact vermijden met: zink, halogenen, niet-metaalachtige oxyhalogeniden, sterk oxiderende middelen, chromylchloride, tementienoliën, nitraten en metaalchloriden.
Automatische ontsteking
356ºF (180ºC).
ontleding
Bij het opwarmen valt het uiteen en geeft het een scherpe en irriterende rook af.
viscositeit
0.2448 cPoise bij 20 ºC.
Warmte van verbranding
8.807 Kcal / g.
Verdampingswarmte
89,8 cal / g bij 30 ºC.
Oppervlaktespanning
17.06 dynes / cm bij 20º C.
Ionisatiepotentieel
9.53 eV.
Geurdrempel
0.83 ppm (zuiverheid wordt niet gegeven).
Brekingsindex
1.355 bij 15 ºC.
verkrijgen
Van ethylalcohol
Ethylether kan worden verkregen uit ethylalcohol, in aanwezigheid van zwavelzuur als een katalysator. Het zwavelzuur in een waterig medium dissocieert het produceren van het hydronium-ion, H3O+.
De watervrije ethylalcohol stroomt door de zwavelzuuroplossing, verwarmd tussen 130 ° C en 140 ° C, waardoor de protonering van ethylalcoholmoleculen wordt geproduceerd. Vervolgens reageert een ander molecuul niet-geprotoneerde ethylalcohol met het geprotoneerde molecuul.
Wanneer dit gebeurt, bevordert de nucleofiele aanval van de tweede molecule van ethylalcohol de afgifte van water uit de eerste molecule (de geprotoneerde); als resultaat wordt een geprotoneerde ethylether gevormd (CH3CH2OHCH2CH3), met gedeeltelijk geladen zuurstofpositief.
Deze methode van synthese verliest echter efficiëntie omdat het zwavelzuur wordt verdund met het water geproduceerd in het proces (product van dehydratie van ethylalcohol).
De temperatuur van de reactie is kritisch. Bij temperaturen onder 130 ° C is de reactie langzaam en voor het grootste deel zal ethylalcohol worden gedistilleerd.
Boven 150 ° C veroorzaakt zwavelzuur de vorming van ethyleen (het alkeen met dubbele binding), in plaats van te combineren met ethylalcohol om ethylether te vormen.
Van ethyleen
In het tegenovergestelde proces, d.w.z. de hydratatie van ethyleen in de dampfase, kan ethylether worden gevormd als een bijproduct naast ethylalcohol. In feite produceert deze synthetische route het grootste deel van deze organische verbinding.
Bij dit proces worden fosforzuurkatalysatoren gebruikt die zijn gefixeerd op een vaste drager en kunnen worden aangepast om meer ether te produceren.
De dehydratie in dampfase van ethanol in de aanwezigheid van aluminiumoxidekatalysatoren kan een opbrengst van 95% bij de productie van ethylether opleveren.
toxiciteit
Het kan irritatie op de huid en ogen veroorzaken door contact. Het contact met de huid kan uitdroging en barsten veroorzaken. De ether dringt meestal niet door de huid, omdat deze snel verdampt.
De irritatie van de ogen veroorzaakt door de ether is meestal mild, en in geval van ernstige irritatie is de schade meestal omkeerbaar.
De inname ervan veroorzaakt narcotische effecten en maagirritatie. Ernstige inname kan nierbeschadiging veroorzaken.
Inademing van de ether kan irritatie van de neus en keel veroorzaken. In het geval van een inademing van ether kan optreden: slaperigheid, opwinding, duizeligheid, braken, onregelmatige ademhaling en verhoogde speekselvloed.
Hoge blootstelling kan verlies van bewustzijn en zelfs de dood veroorzaken.
OSHA stelt een beroepsmatige blootstellingslimiet van gemiddeld 800 ppm vast tijdens een dienst van 8 uur.
Niveaus van oogirritatie: 100 ppm (humaan). Niveaus van oogirritatie: 1200 mg / m3 (400 ppm).
toepassingen
Organisch oplosmiddel
Het is een organisch oplosmiddel dat wordt gebruikt om broom, jodium en andere halogenen op te lossen; de meerderheid van lipiden (vetten), harsen, zuivere rubbers, sommige alkaloïden, gommen, parfums, celluloseacetaat, cellulosenitraat, koolwaterstoffen en kleurstoffen.
Bovendien wordt het gebruikt bij de extractie van de actieve bestanddelen van dierlijke weefsels en planten, omdat het een lagere dichtheid heeft dan water en drijft erop, waardoor de gewenste stoffen in de ether worden opgelost.
Algemene anesthesie
Het werd al sinds 1840 als algemeen verdovingsmiddel gebruikt en vervangt chloroform omdat het een therapeutisch voordeel heeft. Het is echter een ontvlambare stof en ondervindt daarom ernstige problemen voor gebruik in klinische omgevingen.
Bovendien produceert het bij patiënten enkele ongewenste postoperatieve bijwerkingen zoals misselijkheid en braken.
Om deze redenen is het gebruik van ether als een algemene verdoving afgedankt en vervangen door andere anesthetica zoals halothaan..
Geest van de ether
De ether gemengd met ethanol werd gebruikt om de oplossing te vormen die etherether wordt genoemd, die wordt gebruikt bij de behandeling van maagwinderigheid en mildere vormen van gastralgie..
Evaluatie van de bloedsomloop
Ether is gebruikt om de bloedcirculatie tussen een arm en de longen te evalueren. De ether wordt in een arm geïnjecteerd, waardoor het bloed naar het rechter atrium wordt gebracht, vervolgens naar het rechter ventrikel en van daaruit naar de longen.
De tijd die verstrijkt van de injectie van de ether tot de opname van de ethergeur in de uitgeademde lucht, is ongeveer 4 tot 6 seconden..
Onderwijslaboratoria
Ether wordt in veel experimenten gebruikt in onderwijslaboratoria; bijvoorbeeld in de demonstratie van Mendels wetten van de genetica.
De ether wordt gebruikt om de vliegen van het geslacht Drosophila te verdoven en de noodzakelijke kruisingen daartussen mogelijk te maken, om de wetten van de genetica te bewijzen
referenties
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organische chemie. Aminen. (10th editie.). Wiley Plus.
- Carey F. (2008). Organische chemie (Zesde editie). Mc Graw Hill.
- The Sevier. (2018). Diethyl ether. Science Direct. Teruggeplaatst van: sciencedirect.com
- De redacteuren van Encyclopaedia Britannica. (2018). Ethyl ether. Britannica ncyclopædia. Teruggeplaatst van: britannica.com
- PubChem (2018). Ether. Teruggeplaatst van: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Diethyl ether. Teruggeplaatst van: en.wikipedia.org
- Veiligheidsblad XI: ethylether. [PDF]. Hersteld van: quimica.unam.mx


