Calcium Oxide (CaO) structuur, eigenschappen en toepassingen
de calciumoxide (CaO) is een anorganische verbinding die calcium en zuurstof in ionische vormen bevat (niet te verwarren met calciumperoxide, CaO2). Wereldwijd is het bekend als kalk, woord voor alle anorganische verbinding bevattende carbonaten, oxiden en hydroxiden van calcium en andere metalen zoals silicium, aluminium en ijzer.
Dit oxide (of kalk) wordt ook wel aangeduid als ongebluste kalk of gebluste kalk, afhankelijk van het feit of het al dan niet gehydrateerd is. Kalk is calciumoxide, terwijl gebluste kalk het hydroxide is. Op zijn beurt is kalksteen (kalksteen of verharde kalk) eigenlijk een sedimentair gesteente dat voornamelijk bestaat uit calciumcarbonaat (CaCO3).

Het is een van de grootste natuurlijke bronnen van calcium en vormt de grondstof voor de productie van calciumoxide. Hoe wordt dit oxide geproduceerd? Carbonaten zijn gevoelig voor thermische ontbinding; het verwarmen van calciumcarbonaten bij temperaturen boven 825 ° C, leidend tot de vorming van kalk en koolstofdioxide.
De bovenstaande verklaring kan als volgt worden beschreven: CaCO3(s) → CaO (s) + CO2(G). Omdat de aardkorst is rijk aan kalksteen en calciet en oceanen en stranden overvloedig schelpen (grondstof voor de productie van calciumoxide), calciumoxide een relatief goedkope reagentia.
index
- 1 formule
- 2 Structuur
- 3 Eigenschappen
- 3.1 Oplosbaarheid
- 4 Gebruik
- 4.1 Als een mortel
- 4.2 Bij de productie van brillen
- 4.3 In mijnbouw
- 4.4 Als een silicaatverwijderaar
- 5 Nanodeeltjes van calciumoxide
- 6 Referenties
formule
De chemische formule van calciumoxide is CaO, waarin calcium hetzelfde is als het zure ion (elektronacceptor) Ca2+, en zuurstof als het basision (elektronendonor) OR2--.
Waarom calcium +2 oplaadt? Omdat calcium behoort tot groep 2 van het periodiek systeem (Mr Becambara), en slechts twee valentie elektronen vindt bindingvorming, waarbij het zuurstofatoom oplevert.
structuur
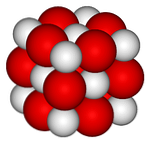
In het bovenste beeld is de kristallijne structuur (gem-zouttype) voor calciumoxide weergegeven. De omvangrijke rode bollen komen overeen met de Ca-ionen2+ en de witte bollen voor de ionen O2-.
In deze kubieke kristallen rangschikking elk ion Ca2+ is omgeven door zes ionen O2-, verstopt in de achtvlakige gaten achtergelaten door grote ionen tussen hen.
Deze structuur is de maximaal ionisch karakter van het oxide, maar het belangrijke verschil van de stralen (rode bol is groter dan de wit) geeft een zwakkere kristalrooster energie vergelijking met MgO.
eigenschappen
Fysiek is het een kristallijne witte vaste stof, geurloos en met sterke elektrostatische interacties, die verantwoordelijk zijn voor zijn hoge smeltpunten (2572 ° C) en koken (2850 ° C). Bovendien heeft het een molecuulgewicht van 55.958 g / mol en de interessante eigenschap dat het thermoluminescent is.
Dit betekent dat een stuk calciumoxide dat aan een vlam wordt blootgesteld, kan schijnen met een intens wit licht, dat in het Engels met de naam bekend is Limelight, of in het Spaans, licht van calcium. De Ca-ionen2+, in contact met het vuur veroorzaken ze een roodachtige vlam, zoals weergegeven in de volgende afbeelding.

oplosbaarheid
CaO is een basisch oxide met een sterke affiniteit voor water, voor zover het vocht absorbeert (het is een hygroscopische vaste stof), en reageert onmiddellijk om gebluste kalk of calciumhydroxide te produceren:
CaO (s) + H2O (l) => Ca (OH)2(S)
Deze reactie is exotherm (laat warmte vrij) als gevolg van de vorming van een vaste stof met sterkere interacties en een stabieler kristalrooster. De reactie is echter omkeerbaar als Ca (OH) wordt verwarmd2, het uitdrogen en het aansteken van de gebluste kalk; dan, de limoen "herboren".
De resulterende oplossing is erg basisch en als het verzadigd is met calciumoxide, bereikt het een pH van 12,8.
Evenzo is het oplosbaar in glycerol en in zuur- en suikeroplossingen. Omdat het een basisch oxide is, heeft het van nature effectieve interacties met zure oxiden (SiO2, de2O3 en geloof2O3, bijvoorbeeld) oplosbaar in de vloeibare fasen daarvan. Aan de andere kant is het onoplosbaar in alcoholen en organische oplosmiddelen.
toepassingen
CaO heeft een uitgebreid groot aantal industriële toepassingen alsook bij de synthese van acetyleen (CH≡CH), het verwijderen van fosfaten uit afvalwater en reactie met zwaveldioxide uit gasvormige afvalstoffen.
Andere toepassingen van calciumoxide worden hieronder beschreven:
Als een mortier
Als het calciumoxide wordt gemengd met zand (SiO2) en water, koeken met het zand en reageert traag met het water om gebluste kalk te vormen. Op zijn beurt, de CO2 van de lucht lost op in het water en reageert met het zout af om calciumcarbonaat te vormen:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
De CaCO3 is een taaier en harder dan de verbinding CaO, waardoor de mortel (het bovenstaande mengsel) uitharden en bevestig de bakstenen, keramische blokken of tussen deze of van de wens.
Bij de productie van brillen
De essentiële grondstof voor de productie van glazen zijn siliciumoxiden, die worden gemengd met kalk, natriumcarbonaat (Na2CO3) en andere additieven, om vervolgens te worden verwarmd, resulterend in een glasachtige vaste stof. Deze vaste stof wordt vervolgens verwarmd en in willekeurige figuren geblazen.
In de mijnbouw
Geslagen kalk neemt een groter volume in dan ongebluste kalk als gevolg van waterstofbinding (O-H-O) interacties. Deze eigenschap wordt gebruikt om de rotsen van binnenuit te breken.
Dit wordt bereikt door ze te vullen met een compact mengsel van kalk en water, dat is verzegeld om de warmte en de expansieve kracht in de rots te concentreren.
Als een silicaatverwijderaar
Het CaO is gesmolten met de silicaten om een coalescentievloeistof te vormen, die vervolgens wordt geëxtraheerd uit de grondstof van een bepaald product.
IJzererts is bijvoorbeeld het ruwe materiaal voor de productie van metaalijzer en -staal. Deze mineralen bevatten silicaten, wat ongewenste onzuiverheden voor het proces zijn en worden geëlimineerd door de zojuist beschreven methode.
Nanodeeltjes van calciumoxide
Calciumoxide kan worden gesynthetiseerd als nanodeeltjes, waarbij de concentraties van calciumnitraat (Ca (NO3)2) en natriumhydroxide (NaOH) in oplossing.
Deze deeltjes zijn bolvormig, basisch (evenals de vaste stof op macroschaal) en hebben veel oppervlakte. Bijgevolg zijn deze eigenschappen gunstig voor de katalytische processen. Wat? De onderzoeken beantwoorden die vraag momenteel.
We gebruikten deze nanodeeltjes om organische verbindingen te synthetiseren zoals gesubstitueerde derivaten piridinas- de ontwikkeling van nieuwe geneesmiddelen voor chemische omzettingen zoals kunstmatige fotosynthese uit te voeren, waterzuivering door zware metalen en schadelijke en als fotokatalytische middelen.
De nanodeeltjes kunnen worden gesynthetiseerd op een biologische drager, zoals de bladeren van papaja en groene thee, om te worden gebruikt als een antibacterieel middel.
referenties
- scifun.org. (2018). Kalk: calciumoxide. Opgehaald op 30 maart 2018, van: scifun.org.
- Wikipedia. (2018). Calciumoxide. Opgehaald op 30 maart 2018, vanaf: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). Groene synthese van calciumoxide-nanodeeltjes en de toepassingen ervan. Int. Journal of Engineering Research and Application. ISSN: 2248-9622, deel 6, nummer 10, (deel -1), pp. 27-31.
- J. Safaei-Ghomi et al. (2013). Calciumoxide-nanodeeltjes gekatalyseerde eenstaps multicomponent-synthese van sterk gesubstitueerde pyridines in waterige ethanolmedium Scientia Iranica, Transacties C: Chemie en chemische techniek 20 549-554.
- PubChem. (2018). Calcium Oxide. Opgehaald op 30 maart 2018, van: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Anorganische chemie in De elementen van groep 2. (vierde editie, pagina 280). Mc Graw Hill.


