Zilveroxide (Ag2O) -structuur, eigenschappen, nomenclatuur en toepassingen
de zilver oxide is een anorganische verbinding waarvan de chemische formule Ag is2O. De kracht die zijn atomen verenigt is van een volledig ionische aard; daarom bestaat het uit een ionische vaste stof waarbij er een verhouding is van twee Ag-kationen+ interactie elektrostatisch met een anion O2-.
Het oxide-anion, O2-, het is het resultaat van de interactie van de zilveratomen van het oppervlak met de zuurstof van de omgeving; op een vergelijkbare manier als ijzer en vele andere metalen. Een zilverstuk of sieraden in plaats van rood worden en afbrokkelen tot roest, wordt zwart, kenmerkend voor zilveroxide.

In de bovenstaande afbeelding ziet u bijvoorbeeld een roestige zilveren kop. Let op het zwart gemaakte oppervlak, hoewel het nog wat sierglans heeft; daarom kunnen zelfs roestige zilveren voorwerpen aantrekkelijk genoeg worden geacht voor decoratief gebruik.
De eigenschappen van zilveroxide zijn zodanig dat ze op het eerste gezicht het originele metalen oppervlak niet bederven. Het wordt gevormd bij kamertemperatuur door eenvoudig contact met de zuurstof in de lucht; en nog interessanter, het kan ontleden bij hoge temperaturen (boven 200 ° C).
Dit betekent dat als het glas van het beeld werd vastgehouden en de hitte van een intense vlam werd toegepast, het zijn zilverachtige glans terugkreeg. Daarom is de vorming ervan een thermodynamisch omkeerbaar proces.
Zilveroxide heeft ook andere eigenschappen en, afgezien van zijn eenvoudige Ag-formule2Of het omvat complexe structurele organisaties en een rijke verscheidenheid aan vaste stoffen. Echter, de Ag2Of is het misschien, naast Ag2O3, de meest representatieve van de oxiden van zilver.
index
- 1 Structuur van zilveroxide
- 1.1 Veranderingen met het aantal valencia
- 2 Fysische en chemische eigenschappen
- 2.1 Molecuulgewicht
- 2.2 Uiterlijk
- 2.3 Dichtheid
- 2,4 Smeltpunt
- 2,5 Kps
- 2.6 Oplosbaarheid
- 2.7 Covalent karakter
- 2.8 Ontleding
- 3 Nomenclatuur
- 3.1 Valencias I en III
- 3.2 Systematische nomenclatuur voor complexe zilveroxiden
- 4 Gebruik
- 5 Referenties
Structuur van zilveroxide
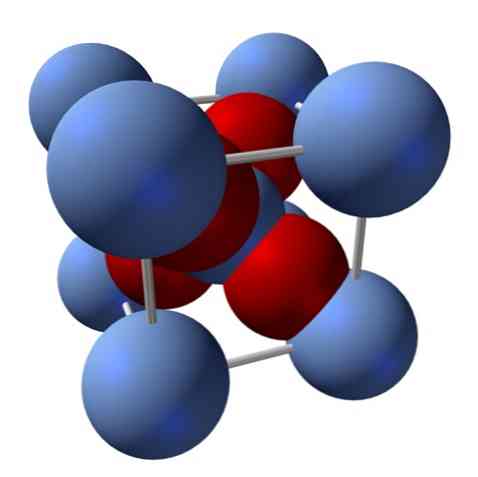
Hoe is de structuur? Zoals vermeld aan het begin: het is een ionische vaste stof. Om deze reden kunnen er geen covalente bindingen Ag-O of Ag = O in de structuur ervan zijn; aangezien, als er waren, de eigenschappen van dit oxide drastisch zouden veranderen. Het zijn dan Ag-ionen+ en O2- in een 2: 1-verhouding en ervaart een elektrostatische aantrekkingskracht.
De structuur van het zilveroxide wordt bepaald door de manier waarop de ionische krachten zich verspreiden in de ruimte van de Ag-ionen+ en O2-.
In het bovenste plaatje, bijvoorbeeld, heb je een eenheidscel voor een kubisch kristallijn systeem: de Ag-kationen+ zijn de zilverblauwe bollen en de O2- de roodachtige bollen.
Als je het aantal bollen meet, zul je merken dat er op het eerste gezicht negen van zilverachtige blauwe en vier rode kleuren zijn. Alleen de fragmenten van de bollen in de kubus worden echter in beschouwing genomen; van het tellen van deze, zijnde fracties van de totale bollen, moet de 2: 1 verhouding voor Ag worden gehaald2O.
Herhaling van de structurele eenheid van de AgO-tetraëder4 omringd door vier andere Ag+, alle zwarte vaste stof is gebouwd (de gaten of onregelmatigheden die deze kristallen arrangementen kunnen hebben, weg te nemen).
Veranderingen met het aantal valencia
Nu niet focussen op de AgO-tetraëder4 maar in de lijn AgOAg (observeer de hoekpunten van de bovenste kubus), zal het zijn dat de vaste zilveroxide uit een ander perspectief bestaat uit meerdere ionlagen die lineair zijn gerangschikt (hoewel hellend). Dit alles als gevolg van de "moleculaire" geometrie rond de Ag+.
Het bovenstaande is bevestigd door verschillende studies van zijn ionische structuur.
Zilver werkt overwegend met valentie +1, omdat bij verlies van een elektron de resulterende elektronische configuratie [Kr] 4d is10, wat erg stabiel is. Andere valenties, zoals Ag2+ en Ag3+ ze zijn minder stabiel omdat ze elektronen verliezen van orbitalen die bijna volledig zijn gevuld.
Het Ag-ion3+, het is echter relatief minder onstabiel in vergelijking met Ag2+. In feite kan het naast elkaar bestaan in het gezelschap van Ag+ Chemisch verrijken van de structuur.
De elektronische configuratie is [Kr] 4d8, met ongepaarde elektronen op een zodanige wijze dat het enige stabiliteit geeft.
In tegenstelling tot lineaire geometrieën rond Ag-ionen+, er is vastgesteld dat die van de Ag-ionen3+ Het is vierkant vlak. Daarom een zilveroxide met Ag-ionen3+ zou bestaan uit lagen bestaande uit AgO-vierkanten4 (geen tetraëders) die elektrostatisch zijn verbonden door AgOAg-lijnen; Dat is het geval van Ag4O4 of Ag2O ∙ Ag2O3 met een monokliene structuur.
Fysische en chemische eigenschappen

Als je het oppervlak van de zilveren beker van de hoofdafbeelding krast, krijg je een effen kleur, die niet alleen zwart is, maar ook bruine of bruine tinten heeft (bovenste afbeelding). Enkele van de fysische en chemische eigenschappen die door de momenten worden gerapporteerd, zijn de volgende:
Moleculair gewicht
231.735 g / mol
verschijning
Stevig zwartbruin in poedervorm (merk op dat het, ondanks dat het een ionische vaste stof is, een kristallijn uiterlijk heeft). Het is geurloos en vermengd met water geeft het een metaalachtige smaak
dichtheid
7,14 g / ml.
Smeltpunt
277-300 ° C. Zeker, het smelt in vast zilver; dat wil zeggen, het breekt waarschijnlijk af vóór het vormen van vloeibaar oxide.
kps
1,52 ∙ 10-8 in water bij 20 ° C. Het is daarom een verbinding die nauwelijks oplosbaar is in water.
oplosbaarheid
Als je goed naar het beeld van zijn structuur kijkt, zul je merken dat de sferen van Ag2+ en O2- Ze zijn het niet oneens bijna in grootte. Dientengevolge kunnen alleen kleine moleculen het binnenste van het kristallijne rooster doordringen, waardoor het in bijna alle oplosmiddelen onoplosbaar wordt; behalve degene waar het reageert, zoals basen en zuren.
Covalent karakter
Hoewel er herhaaldelijk is gezegd dat zilveroxide een ionische verbinding is, zijn bepaalde eigenschappen, zoals het lage smeltpunt, in tegenspraak met deze verklaring.
Zeker, de overweging van het covalente karakter breekt niet af wat wordt uitgelegd voor zijn structuur, het zou voldoende zijn om het toe te voegen aan de structuur van Ag.2Of een model van bollen en staven om covalente banden aan te duiden.
Ook de tetraëders en vierkante vlakken AgO4, evenals de AgOAg-lijnen, zouden ze verbonden zijn door covalente (of covalente ionische) bindingen.
Met dit in gedachten, de Ag2Of het zou eigenlijk een polymeer zijn. Het wordt echter aanbevolen om het te beschouwen als een ionische vaste stof met een covalent karakter (de aard van de link is tegenwoordig nog steeds een uitdaging).
ontleding
In het begin werd vermeld dat de vorming ervan thermodynamisch omkeerbaar is, dus absorbeert het warmte om terug te keren naar de metaaltoestand. Dit alles kan worden uitgedrukt door twee chemische vergelijkingen voor dergelijke reacties:
4Ag (s) + O2(g) => 2Ag2O (s) + Q
2AG2O (s) + Q => 4Ag (s) + O2(G)
Waarbij Q de warmte in de vergelijking vertegenwoordigt. Dit verklaart waarom het vuur dat het oppervlak van de geroeste zilveren kop brandt, zijn zilveren glans terugkrijgt.
Daarom is het moeilijk om aan te nemen dat er Ag is2O (l) omdat het onmiddellijk zou ontbinden door warmte; tenzij de druk te hoog is om de bruinzwarte vloeistof te verkrijgen.
nomenclatuur
Toen de mogelijkheid van Ag-ionen werd geïntroduceerd2+ en Ag3+ naast de gemeenschappelijke en overheersende Ag+, de term 'zilveroxide' lijkt onvoldoende te lijken om naar Ag te verwijzen2O.
Dit komt omdat het Ag-ion+ is overvloediger dan de anderen, dus de Ag wordt genomen2Of als het enige oxide; wat helemaal niet klopt.
Als je de Ag2+ omdat deze vrijwel onbestaand is vanwege zijn instabiliteit, zullen alleen de ionen met valenties +1 en +3 aanwezig zijn; dat wil zeggen Ag (I) en Ag (III).
Valencias I en III
Omdat het de Ag (I) de minste valentie is, wordt het genoemd door het achtervoegsel -oso aan zijn naam toe te voegen Argentum. Dus de Ag2Of het is: argentoso-oxide of, volgens de systematische nomenclatuur, diplomatmonoxide.
Als Ag (III) volledig wordt genegeerd, moet de traditionele nomenclatuur zijn: zilveroxide in plaats van argentineoxide.
Aan de andere kant is de Ag (III) de grootste valentie waaraan het achtervoegsel -ico is toegevoegd. Dus de Ag2O3 is: zilveroxide (2 Ag-ionen)3+ met drie O2-). Ook zou de naam ervan volgens de systematische nomenclatuur zijn: diplatatrioxide.
Als de structuur van Ag wordt waargenomen2O3, het kan worden verondersteld dat het het product is van oxidatie door ozon, OF3, in plaats van zuurstof. Daarom moet het covalente karakter ervan groter zijn omdat het een covalente verbinding is met Ag-O-O-O-Ag of Ag-O-bindingen.3-ag.
Systematische nomenclatuur voor complexe zilveroxiden
De AgO, ook geschreven als Ag4O4 of Ag2O ∙ Ag2O3, het is een zilveroxide (I, III), omdat het beide valenties +1 en +3 heeft. De naam ervan volgens de systematische nomenclatuur zou zijn: tetraplatetetraoxide.
Deze nomenclatuur is van grote hulp als het gaat om andere stoichiometrisch complexere zilveroxiden. Stel bijvoorbeeld dat de twee vaste stoffen 2Ag2O ∙ Ag2O3 en Ag2O ∙ 3Ag2O3.
Het schrijven van de eerste op een meer geschikte manier zou zijn: Ag6O5 (het tellen en optellen van de atomen van Ag en O). Zijn naam zou dan hexaplaat pentoxide zijn. Merk op dat dit oxide een zilverpreparaat heeft dat minder rijk is dan Ag2O (6: 5 < 2:1).
Tijdens het schrijven van de tweede solid anders zou het zijn: Ag8O10. De naam zou octaplaat-decaoxide zijn (met een verhouding van 8:10 of 4: 5). Dit hypothetische zilveroxide zou "zeer geoxideerd" zijn.
toepassingen
Studies die op zoek zijn naar nieuwe en geavanceerde toepassingen voor zilveroxide worden nog steeds uitgevoerd. Enkele van de toepassingen worden hieronder vermeld:
-Het wordt opgelost in ammoniak, ammoniumnitraat en water om het Tollens-reagens te vormen. Dit reagens is een nuttig hulpmiddel bij kwalitatieve analyses in organische chemielaboratoria. Het maakt het mogelijk de aanwezigheid van aldehyden in een monster te bepalen, waarbij de positieve reactie de vorming van een "zilveren spiegel" in de reageerbuis is..
-Samen met het metaalzink vormt het de primaire batterijen van zinkoxide van zilver. Dit is misschien een van de meest voorkomende en huiselijke toepassingen.
-Het dient als een gaszuiveraar en absorbeert bijvoorbeeld CO2. Wanneer het wordt opgewarmd, laat het de ingesloten gassen vrij en kan het meerdere keren worden hergebruikt.
-Vanwege de antimicrobiële eigenschappen van zilver is het oxide ervan nuttig in studies van bioanalyse en bodemzuivering.
-Het is een mild oxidatiemiddel dat in staat is tot het oxideren van aldehyden tot carbonzuren. Het wordt ook gebruikt in de Hofmann-reactie (tertiaire amines) en neemt deel aan andere organische reacties, hetzij als reagens of katalysator.
referenties
- Bergstresser M. (2018). Silver Oxide: Formula, Decomposition & Formation. Study. Teruggeplaatst van: study.com
- Auteurs en editors van de volumes III / 17E-17F-41C. (N.D.). Zilveroxiden (Ag (x) O (y)) kristalstructuur, roosterparameters. (Numerieke gegevens en functionele relaties in wetenschap en technologie), deel 41C. Springer, Berlijn, Heidelberg.
- Mahendra Kumar Trivedi, Rama Mohan Tallapragada, Alice Branton, Dahryn Trivedi, Gopal Nayak, Omprakash Latiyal, Snehasis Jana. (2015). Het potentiële effect van bioveld energietherapie op de fysische en thermische eigenschappen van zilveroxidepoeder. International Journal of Biomedical Science and Engineering. Deel 3, nr. 5, blz. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Ontleding van zilveroxide. Universiteit van Oregon Teruggeplaatst van: chemdemos.uoregon.edu
- Flint, Deyanda. (24 april 2014). Gebruik van zilveroxidebatterijen. Sciencing. Teruggeplaatst van: sciencing.com
- Salman Montasir E. (2016). Studie van enkele optische eigenschappen van zilveroxide (Ag2o) met behulp van UV-zichtbare spectrofotometer. [PDF]. Teruggeplaatst van: iosrjournals.org
- Bard Allen J. (1985). Standaardpotentialen in waterige oplossing. Marcel Dekker. Opgehaald van: books.google.co.ve


