Streptococcus sanguinis kenmerken, morfologie en levenscyclus
de Streptococcus sanguinis, voorheen bekend als Streptococcus sanguis, is een facultatieve Gram-positieve anaerobe bacterie die deel uitmaakt van de tandplak. Onder normale omstandigheden komt het in de mond voor omdat het de mogelijkheid heeft om aan het speeksel te hechten door interactie met eiwitten op het tandoppervlak.
Het is antagonistisch voor andere soorten van het geslacht die pathogenen kunnen zijn, zoals S. mutans, de belangrijkste bacterie die cariës bevordert..
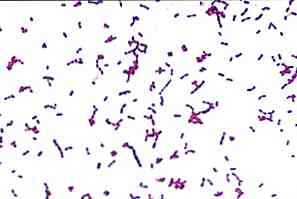
Streptococcus is een geslacht van Gram-positieve bacteriën, waaronder we een grote verscheidenheid aan soorten vinden die al dan niet pathogeen zijn voor het menselijk lichaam.
Deze diverse groep micro-organismen worden genoemd bacteriën die behoren tot de orale of darmflora van mensen en hebben gunstige functies lichaamshomeostase, zoals de controle van pathogene micro-organismen en de productie van moleculen die op fysiologische activiteiten. Onder hen vinden we S. sanguinis, bacteriën in de mondholte.
index
- 1 Is het pathogeen?
- 2 Biologische kenmerken
- 3 Morfologie
- 4 Levenscyclus
- 5 Symptomen van infectie
- 6 Behandeling tegen infectieuze endocarditis veroorzaakt door streptococci van de viridansgroep
- 7 Diagnostische methoden voor de identificatie van endocarditis veroorzaakt door S. sanguinis
- 8 Referenties
Is het pathogeen?
Onder normale omstandigheden is deze bacterie niet pathogeen, hoewel er bij verandering van de homeostase in het lichaam een afname van de populatie kan zijn..
Dit maakt de mondholte kwetsbaar voor invasie door S. mutans en andere pathogenen zoals Prevotella internedia, die gingivitis en parodontitis veroorzaakt..
Bovendien is S. sanguinis een van de hoofdoorzaken van infectieuze endocarditis van de oorspronkelijke klep. Deze pathologie treedt op vanwege de endovasculaire infectie van de hartstructuren die in contact staan met de bloedstroom.
Biologische eigenschappen
S. sanguinis is een facultatieve Gram-positieve anaerobe bacterie, behorende tot de groep van S. viridans.
Deze bacterie is anaëroob, omdat het hebben van het vermogen om te overleven zonder zuurstof, echter, zijn facultatief, hebben het grote vermogen om zuurstof te gebruiken in hun metabolische processen voor vergisting, zonder dat het giftig voor haar.
S. sanguinis is een Gram-positieve bacterie, gekenmerkt door de aanwezigheid van een cellulaire envelop gevormd door een cytoplasmatisch membraan en een dikke celwand samengesteld uit peptidoglycanen.
Deze twee lagen worden verbonden door de verbinding van lipoteichoïnezuurmoleculen. Anders dan gramnegatief, hebben peptidoglycanen met celwand in Gram-positieve bacteriën het vermogen om de kleurstof te behouden tijdens Gram-kleuring, waardoor de donkerblauwe of violette bacteriën zichtbaar zijn.
Het belangrijkste kenmerk van S. viridans streptococci van de groep is dat ze alfa-hemolytische, betekent dat alfa-hemolyse veroorzaken op bloed agar, waar we de vorming van een groene ring rond de kolonie observeren.
Dit proces is voornamelijk te wijten aan de oxidatie van hemoglobine in erytrocyten door de afscheiding van waterstofperoxide (H2O2).
Het vermogen van deze bacterie om zich te hechten aan de speekselomhulling en het tandoppervlak is te wijten aan de affiniteit van de componenten van het membraan aan componenten van speeksel zoals immunoglobuline A en alfa-amylase..
morfologie
De morfologie van de viridans-groepstreptokokken is erg basaal. Bacteriën van dit geslacht hebben een afgeronde vorm, met een gemiddelde grootte van 2 micrometer in diameter en zijn gegroepeerd in paren of middellange of lange ketens, hebben geen capsule en zijn niet gesporuleerd..
Deze bacteriën vertonen een grijsgroene kleuring, en presenteren het celmembraan en de celwand samengesteld uit peptidoglycanen, die verantwoordelijk zijn voor het behouden van de vlek in de Gram-kleuring..
De viridansgroepbacteriën hebben adhesiestructuren in het celmembraan, waaronder de fimbrias en adhesines, verantwoordelijk voor binding aan specifieke receptoren van dentale film.
Levenscyclus
Deze bacterie in de dentale biofilm, met goedaardig gedrag onder normale omstandigheden, maakt samen met 700 andere soorten bacteriën deel uit van de normale flora van de menselijke mondholte.
Begint zijn kolonisatiecyclus tussen 6 en 12 maanden van het menselijk leven en zijn organisatie in het tandvlees begint met het verschijnen van het eerste gebitsstuk.
S sanguinis wordt geassocieerd met de gezonde biofilm en door de productie van glucosyltransferase worden de lucanen gesynthetiseerd, sucrose hydrolyserend en glucoseresten overgebracht.
Het proces van adhesie aan de biofilm wordt gegeven door fimbrias en adhesines. Deze moleculen aanwezig in het bacteriële oppervlak binden met specifieke receptoren in de componenten van speeksel en tanden.
Een bacterie zijn van de orale flora-kolonisatie is normaal en gematigd, en zijn verschijning in de biofilm is een indicator voor de mondgezondheid. De afname ervan is geassocieerd met het verschijnen van ziekteverwekkers zoals S. mutans, die het verschijnen van cariës bevorderen.
Symptomen van infectie
In het geval van de aanwezigheid van dit organisme in de mondholte, zijn er geen symptomen die kenmerkend zijn voor een pathologie, omdat S. sanguinis een goedaardige bacterie is die deel uitmaakt van de normale flora van de mond. Wanneer dit echter de oorzaak is van infectieuze endocarditis, treden er verschillende symptomen op..
Infectieuze endocarditis is een endovasculaire wijziging, namelijk het endocardium, veroorzaakt door verschillende pathogenen, waaronder S. aureus gevonden, S pneumoniane en viridans streptococci.
In het geval van S. sanguinis, hebben symptomen het begin van de infectie, meer of minder dan zes weken verschijning vertraagd, met een stille evolutie, dat is pijnloos en kan worden verward met andere vormen van hart-en vaatziekten, in het bijzonder wanneer de patiënt heeft een eerdere hartaandoening.
Vervolgens kunnen langdurige koortsachtige pieken, vermoeidheid, zwakte, gewichtsverlies en hartfalen worden gezien. Complicaties kunnen optreden als splenomegalie, die is gebaseerd op de toename levergrootte die atrofie van het orgaan, hemorragische manifestaties trombotische, cutane manifestaties, bloedingen veroorzaakt in verschillende gebieden van het lichaam (handen, voeten, ogen), neurologische aandoeningen , zoals cerebrale trombose, hemiplegie en psychotische symptomen, onder anderen.
Behandeling tegen infectieuze endocarditis veroorzaakt door streptococci van de viridansgroep
In de hoofdbehandeling is het gebruik van antibiotica die geen weerstand bieden tegen bacteriën. Het gebruik van antibiotica is afhankelijk van de voortgang van de infectie, bij normale afbeeldingen wordt 4 tot 6 weken gegeven.
Verschillende onderzoeken hebben aangetoond dat streptokokken uit de viridansgroep, waaronder S. sanguinis, gevoelig zijn voor penicilline. Om deze reden wordt de behandeling voor de infectie uitgevoerd met een combinatie van penicilline met andere antibiotica zoals gentamicine, vancomycine en ceftriaxon..
Diagnostische methoden voor de identificatie van endocarditis veroorzaakt door S. sanguinis
De belangrijkste diagnostische methode om de oorzaak van infectieuze endocarditis door S. sanguinis en in het algemeen door een ander pathogeen gerelateerd aan de pathologie te bepalen, is door middel van demonstratie door kweek of histopathologie van het hartabces..
De gebruikelijke laboratoriumstudies die worden uitgevoerd samen met histopathologische tests zijn:
-Leverbiometrie, acute fase reactanten zoals C-reactief proteïne om ontstekingsaandoeningen, nier- en leverfunctie, algemene urinalyse en bloedkweken aan te geven.
-Bovendien zijn thoraxfoto's en echocardiogrammen voor het zoeken naar myocard-abcessen of trombi zeer nuttig bij de diagnose.
referenties
- Socransky, S. S., Manganiello, A., Propas, D., Oram, V. en Houte, J. (1977). Bacteriologische studies van het ontwikkelen van supragingivale tandplak. Journal of Periodontal Research, 12: 90-106.
- Maeda, Y., Goldsmith, C.E., Coulter, W.A., Mason, C., Dooley, J.S. G., Lowery, C.J., & Moore, J.E. (2010). De viridans groeperen streptokokken. Beoordelingen in Medische microbiologie, 21 (4).
- Truper, H. en. L. D. Clari. 1997. Taxonomische noot: noodzakelijke correcties van specifieke epitheta gevormd als substantives (zelfstandige naamwoorden) "in apposition". Int. J. Syst. Bacteriol. 47: 908-909.
- Caufield, P.W., Dasanayake, A.P., Li, Y., Pan, Y., Hsu, J., & Hardin, J.M. (2000). Natuurlijke geschiedenis van Streptococcus sanguinis in de mondholte van zuigelingen: bewijs voor een discreet venster van infectie. Infection and Immunity, 68 (7), 4018 LP-4023.
- Xu, P., Alves, J.M., Kitten, T., Brown, A., Chen, Z., Ozaki, L.S., ... Buck, G. A. (2007). Genoom van de opportunistische pathogeen Streptococcus sanguinis. Journal of Bacteriology, 189 (8), 3166-3175.
- Hernadez, F.H. (2016). Interactie van Streptococcus sanguinis in de levensvatbaarheid en groei van Candida albicans in de mondholte. University of Chile, Faculteit der Tandheelkunde. Toegewezen aan onderzoeksproject: PRI-ODO 2016 04/016
- Handleiding voor de behandeling van infectieuze endocarditis. (2011). Kinderziekenhuis van Mexico Federico Gomez. Afkomstig van himfg.com.mx.
- Edwin & Jessen. (). BIOCHEMIE EN MILIEU-MICROBIOLOGIE. Helaas Peruaanse universiteit.
- Sánchez C. M. A, González, T. F, Ayora, T.T. R, Martínez, Z.E., Pacheco, N. A. L (2017). Wat zijn de micro-organismen Science. 68 (2).
- Ramos, P. D., & Brañez, K. (2016). Stinptococcus Sanguinis en Actinomyces Viscosus Baanbrekende bacteriën in de vorming van biofilmtandheelkunde. Kiru Magazine, 13 (2), 179-184.
- Ge, X. T., Kitten, Z., Chen, S.P., Lee, C.L., Munro., Xu, P. (2008). Identificatie van Streptococcus sanguinis-genen die nodig zijn voor biofilmvorming en onderzoek naar hun rol bij virulentie bij endocarditis. (76), 2251- 2259.
- .


