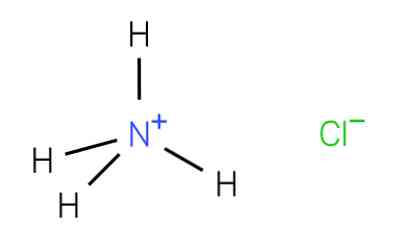
Ammoniumchloride (NH4Cl) Formule, eigenschappen, risico's en toepassingen
de ammoniumchloride, ook bekend als ammoniakzout, is een anorganisch zout dat wordt aangetroffen in urine waarvan de formule NH is4Cl. Het wordt gevonden in mineralogische formaties en in deze vorm wordt ammoniakzout genoemd. Het is ook gevonden in sommige vulkanische openingen en as.
Het kan op verschillende manieren worden verkregen. De eerste is door de neutralisatie met HC1 van het ammoniakale residu gevormd bij de destillatie van kool: NH3 + HCl → NH4cl.
De tweede strategie is via het Solvay-proces om natriumcarbonaat (of bicarbonaat) te verkrijgen en waar ammoniumchloride wordt geproduceerd als een bijproduct:
NH3 + CO2 + NaCl + H2O → NH4Cl + NaHCO3
Bij het Solvay-proces wordt natriumbicarbonaat teruggewonnen door filtratie en vervolgens kristalliseert het ammoniumchloride dat in oplossing blijft (Ammonium Chloride Formula, S.F.).
Meer dan 230.000 ton ammoniumchloride wordt jaarlijks geproduceerd in Japan, waar het voornamelijk wordt gebruikt als meststof in de rijstteelt.
Het geurloze zout heeft echter vele andere toepassingen die het gebruik bij de vervaardiging van persoonlijke reinigingsproducten, pyrotechniek, als een component in de metallurgische industrie, medicijnen, als smaakstof in de voedselindustrie en als een elektrolyt in zinkbatterijen omvatten. -carbon (The Chemical Company, 2016).
index
- 1 Fysische en chemische eigenschappen
- 2 Reactiviteit en gevaren
- 3 Gebruik
- 3.1 1- Geneeskunde
- 3.2 2- Meststof
- 3.3 3- Metallurgie
- 3.4 4- Batterijcomponent
- 3.5 5- Lunch
- 3.6 6- Andere toepassingen
- 4 Referenties
Fysische en chemische eigenschappen
Ammoniumchloride zijn hygroscopische, fijnverdeelde, geurloze witte deeltjes (Nationaal centrum voor biotechnologische informatie., 2017).

De verbinding heeft een trikliene netwerkstructuur met een kubieke structuur gecentreerd in het midden. Het molecuulgewicht is 53.490 g / mol, de dichtheid is 1,5274 g / ml en het smelt- en kookpunt is 338 ºC en 520 ºC.
Ammoniumchloride is oplosbaar in water en kan 383,0 g verbinding per liter oplosmiddel oplossen. Het is ook oplosbaar in ethanol, methanol en glycerol en enigszins oplosbaar in aceton. Het is onoplosbaar in organische oplosmiddelen zoals ethylacetaat (Royal Society of Chemistry, 2015).
Ammoniumchloride kan verschillende reacties ondergaan die van grote waarde zijn voor de chemische en farmaceutische industrie. Het kan ontbinden wanneer verwarmd in zoutzuur en ammoniak:
NH4Cl → NH3 + HCl
Bovendien kan het reageren met basen zoals natrium- of kaliumhydroxide om ook ammoniakgas te produceren:
NH4Cl + NaOH → NH3 + NaCl + H2O
Een andere belangrijke reactie waarbij ammoniakchloride wordt gebruikt, is de afbraak van carbonaten en bicarbonaten, waarbij een zout en ammoniak worden gevormd:
2NH4Cl + Na2CO3 → 2NaCl + CO2 + H2O + 2NH3
Ammoniumchloride wordt als een zuur zout beschouwd. De resulterende oplossingen bevatten matige concentraties aan hydroniumionen en hebben een pH van minder dan 7,0. Reageer als zuren om basen te neutraliseren.
Over het algemeen reageren ze niet als oxidatiemiddelen of reductiemiddelen, maar dergelijk gedrag is niet onmogelijk. Veel van deze verbindingen katalyseren organische reacties (ammoniumchloride, 2016).
Reactiviteit en gevaren
Ammoniumchloride is extreem giftig en giftig. Het veroorzaakt schade aan organen door inslikken of langdurige blootstelling en is ook schadelijk voor de ogen. Het is niet ontvlambaar en reageert niet met andere chemicaliën (Het Nationaal Instituut voor veiligheid en gezondheid, 2014).
In geval van contact met de ogen, moet u controleren of u contactlenzen draagt en deze onmiddellijk verwijderen. De ogen moeten gedurende ten minste 15 minuten worden gespoeld met stromend water, waarbij de oogleden open blijven. Je kunt koud water gebruiken. Zalf mag niet voor de ogen worden gebruikt.
Als de chemische stof in contact komt met kleding, verwijder deze dan zo snel mogelijk en bescherm uw eigen handen en lichaam.
Plaats het slachtoffer onder een veiligheidsdouche. Als de chemische stof zich ophoopt op de blootgestelde huid van het slachtoffer, zoals de handen, wast deze de verontreinigde huid voorzichtig met stromend water en niet-schurende zeep. Je kunt koud water gebruiken. Als irritatie aanhoudt, medische hulp inroepen. Verontreinigde kleding wassen voor hergebruik.
Als het contact met de huid ernstig is, moet het worden gewassen met een ontsmettingsmiddel en de huid bedekken die is verontreinigd met een antibacteriële crème..
In geval van inademing moet het slachtoffer in een goed geventileerde ruimte kunnen verblijven. Als de inademing ernstig is, moet het slachtoffer zo snel mogelijk worden geëvacueerd naar een veilige plaats. Maak strak zittende kleding los, zoals de overhemdkraag, riemen of stropdas.
Als het slachtoffer moeite heeft om te ademen, moet zuurstof worden toegediend. Als het slachtoffer niet ademt, wordt een mond-op-mond reanimatie uitgevoerd. Altijd rekening houdend met het feit dat het voor de hulpverlener gevaarlijk kan zijn om mond-op-mondbeademing te geven wanneer het geïnhaleerde materiaal giftig, infectueus of bijtend is.
In geval van inslikken, niet laten braken. Maak strak zittende kleding los, zoals halsbanden, riemen of stropdassen. Als het slachtoffer niet ademt, voer dan mond-op-mond-reanimatie.
In alle gevallen dient u onmiddellijk medische hulp in te roepen (Material Safety Data Sheet Ammonium chloride, 2013).
toepassingen
1- Geneesmiddel
Ammoniumchloride heeft een zeer belangrijke biochemische functie: het behoudt de fysiologische pH.
Als een zuur zout kan het helpen situaties te corrigeren waarin de plasmaconcentratie van chloride-ionen laag is of in geval van bloedalkalose (hoge bloed-pH). Dit kan optreden na braken, afzuiging (verwijdering) van de maaginhoud, gebruik van diuretica (water of vloeibare pillen) of met bepaalde maagaandoeningen.
Ammoniumchloride veroorzaakt ook de eliminatie van overtollige zouten en water door meer urineren en veroorzaakt acidose in de urine (maakt het zuurter).
Ammoniumchloride is ook gebruikt om zwelling of gewichtstoename die vóór de menstruatie optreedt te verminderen en als hulpmiddel bij de behandeling van urineweginfecties (University of Utah, 2017).
Het is een bestanddeel van veel verkoudheids- en hoestmiddelen vanwege zijn effectiviteit als slijmoplossend middel. In de diergeneeskunde wordt het gebruikt om urinestenen bij geiten, runderen en schapen te voorkomen (Encyclopædia Britannica, 2016).
2- Kunstmest
Ammoniumchloride wordt voornamelijk gebruikt als stikstofbron in meststoffen (die overeenkomt met 90% van de wereldproductie van de verbinding), zoals fosfaat cloroamonio vooral voor rijst en tarwe gewassen in Azië.
3- Metallurgie
Ammoniumchloride wordt gebruikt als een flux bij de bereiding van metalen die moeten worden gecoat met tin, gegalvaniseerd of gelast. Het werkt als een flux door het oppervlak van de werkstukken te reinigen door te reageren met de metaaloxiden op het oppervlak om een vluchtig metaalchloride te vormen.
Om dit te doen, wordt het verkocht in blokken in ijzerhandel voor gebruik bij het reinigen van de punt van een soldeerbout, en kan het in het soldeersel worden opgenomen als een flux.
4- Batterijcomponent
Ammoniumchloride, NH4Cl, is een component van droge celbatterijen, energiereservoirs die elektrische apparaten van stroom voorzien. Met batterijen kunt u elektriciteit gebruiken als u niet in de buurt van een stopcontact of stopcontact bent.
Er zijn drie hoofdcomponenten voor elke batterij: een kathode (de bovenkant van je AA-batterij, waaruit elektronen stromen), een anode (de onderkant van de AA-batterij waarnaar elektronen stromen) en een elektrolyt om waardoor elektronen en ionen kunnen bewegen.
Wanneer ammoniumchloride wordt gebruikt als een elektrolyt in een batterij, wordt het een waterige pasta en wordt het geplaatst tussen de kathode en de anode.
De chemische reacties tussen de batterijkathodes en de anodes zorgen ervoor dat de elektronen door de ammoniumchloridepasta stromen, weg van de kathode en in de richting van de anode.
De elektronen passeren de metalen contacten in het batterijcompartiment waardoor de elektrische apparatuur werkt (American Chemistry Council, Inc., 2005).
5- Eten
In verschillende landen wordt ammoniumchloride, onder de naam ammoniakzout of informeel salmiakki, gebruikt als een levensmiddelenadditief onder het nummer E E510, meestal als een gistvoedingsstof in de broodproductie.
Het is een voedingssupplement voor vee en een ingrediënt in voedzame media voor gisten en vele micro-organismen.
Ammoniumchloride wordt gebruikt om donkere snoepjes op smaak te brengen die zoute drop worden genoemd (erg populair in Scandinavische landen), om te bakken om koekjes een zeer knapperige textuur te geven, en in Salmiakki Koskenkorva-likeur om te aromatiseren.
In India en Pakistan wordt het "Noshader" genoemd en wordt het gebruikt om de versheid van sandwiches zoals samosa's en jalebi te verbeteren..
6- Andere toepassingen
Ammoniumchloride te vinden in shampoo, haarverf en bleekmiddelen, reinigingsmachinelichaam en wassen, gezichtsreiniger, conditioner, afwasmiddel, alsmede badoliën en zouten.
Ammoniumchloride wordt ook gebruikt bij het etsen bij de vervaardiging van gedrukte schakelingen, zoals een brandblusser. Het is ook een ingrediënt in vuurwerk, explosieven en lucifers en als een uithardingsmiddel in lijmen op basis van formaldehyde.
referenties
- American Chemistry Council, Inc. (2005, mei). Ammoniumchloride: Helpt draagbare elektriciteit te leveren. Hersteld van americanchemistry: americanchemistry.com.
- Ammoniumchloride. (2016). Opgehaald van CAMEO Chemicals: cameochemicals.noaa.gov.
- Ammoniumchloride Formule. (S.F.). Hersteld van softschools: softschools.com.
- EMBL-EBI. (2016, 29 februari). ammoniumchloride. Hersteld van ChEBI: ebi.ac.uk.
- Encyclopædia Britannica. (2016, 13 april). Ammoniumchloride (NH4Cl). Teruggeplaatst van Encyclopædia Britannica: britannica.com.
- Veiligheidsinformatieblad Ammoniumchloride. (2013, 21 mei). Herstelde desciencelab: sciencelab.com.
- Nationaal centrum voor informatie over biotechnologie. (2017, 22 april). PubChem Compound-database; CID = 25517. Opgehaald van PubChem: pubchem.ncbi.nlm.nih.gov.
- Royal Society of Chemistry. (2015). Ammoniumchloride. Opgehaald van chemspider: chemspider.com.
- The Chemical Company. (2016). Ammoniumchloride. Hersteld van thechemco: thechemco.com.
- Het nationale instituut voor veiligheid en gezondheid op het werk. (2014, 1 juli). AMMONIUMCHLORIDE. Hersteld van cdc.gov.
- Universiteit van Utah (2017). Ammonium Chloride maagsapresistente tabletten. RRecuperado dehealthcare.utah.edu.


