Theory of Bands Model en voorbeelden
de band theorie is er een die de elektronische structuur van de vaste stof als geheel definieert. Het kan worden toegepast op elk type vaste stof, maar het bevindt zich in de metalen waar zijn grootste successen worden weerspiegeld. Volgens deze theorie is de metaalbinding het gevolg van de elektrostatische aantrekking tussen de positief geladen ionen en de mobiele elektronen in het kristal.
Daarom heeft het metaalkristal een "zee van elektronen", die de fysische eigenschappen ervan kan verklaren. Het onderste beeld illustreert de metalen link. De paarse stippen van de elektronen worden gedelocaliseerd in een zee die de positief geladen metaalatomen omhult.

De "zee van elektronen" wordt gevormd door de individuele bijdragen van elk metaalatoom. Deze bijdragen zijn de atoomorbitalen. De metalen structuren zijn over het algemeen compact; hoe compacter ze zijn, hoe groter de interacties tussen hun atomen.
Als gevolg hiervan overlappen hun atomaire orbitalen elkaar om zeer smalle moleculaire orbitalen in energie te genereren. De zee van elektronen is dan slechts een grote verzameling moleculaire orbitalen met verschillende energiegebieden. Het bereik van deze energieën vormt wat bekend staat als energiebanden.
Deze banden zijn aanwezig in elke regio van het kristal, daarom wordt het als een geheel beschouwd en van daaruit komt de definitie van deze theorie.
index
- 1 Model van energiebanden
- 1.1 Fermieniveau
- 2 Halfgeleiders
- 2.1 Intrinsieke en extrinsieke halfgeleiders
- 3 Voorbeelden van toegepaste bandentheorie
- 4 Referenties
Energy bands model

Wanneer de s orbital van een metaalatoom reageert met de buren (N = 2), twee moleculaire orbitalen worden gevormd: één schakel (groene markering) en andere antibindende (donkerrood band).
Als N = 3, worden nu drie moleculaire orbitalen gevormd, waarvan de middelste (zwarte band) niet-bindend is. Als N = 4, worden vier orbitalen gevormd en degene met het grootste bindende karakter en degene met het grootste antivrieskarakter worden verder gescheiden.
Het bereik van beschikbare energie voor moleculaire orbitalen wordt groter naarmate de metaalatomen van het kristal hun orbitalen leveren. Dit resulteert ook in een afname van de energieruimte tussen de orbitalen, tot het punt dat ze in een band condenseren.
Deze band bestaat uit orbitalen met gebieden met lage energie (die van groene en gele kleuren) en hoge energie (die van oranje en rode kleuren). Hun energetische uitersten hebben een lage dichtheid; de meeste moleculaire orbitalen (witte streep) zijn echter geconcentreerd in het midden.
Dit betekent dat elektronen "sneller rennen" door het midden van de band dan aan hun uiteinden.
Fermi niveau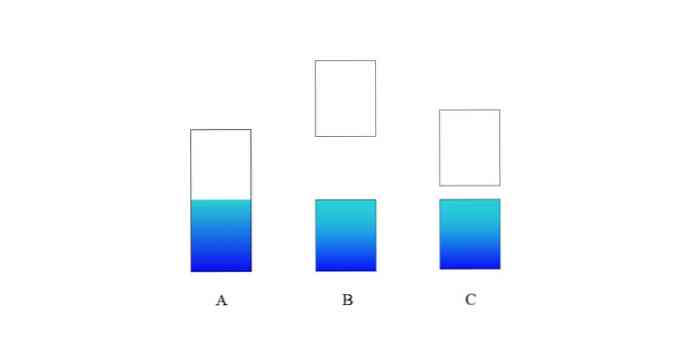
Het is de hoogste energietoestand ingenomen door elektronen in een vaste stof bij de absolute nultemperatuur (T = 0 K).
Zodra de band is gebouwd, beginnen de elektronen al hun moleculaire orbitalen te bezetten. Als het metaal één valentie-elektron (en) heeft1), alle elektronen in zijn kristal zullen de helft van de band innemen.
De andere onbezette helft staat bekend als de drijvende band, terwijl de band vol met elektronen de valentieband wordt genoemd.
In het bovenste beeld staat A voor een typische valentieband (blauw) en geleidingsband (wit) voor een metaal. De blauwachtige grenslijn geeft het niveau van Fermi aan.
Omdat metalen ook p-orbitalen hebben, combineren ze op dezelfde manier om een p-band (wit) te maken.
In het geval van metalen zijn de s- en p-banden zeer dicht bij elkaar. Dit maakt overlappingen mogelijk, waarbij elektronen uit de valentieband naar de geleidingsband worden bevorderd. Dit gebeurt zelfs bij temperaturen van iets meer dan 0 K.
Voor de overgangsmetalen en vanaf periode 4 naar beneden, is het ook mogelijk om banden te vormen van.
Het niveau van Fermi ten opzichte van de geleidingsband is erg belangrijk om de elektrische eigenschappen te bepalen.
Bijvoorbeeld een metaal Z een Fermi niveau dichtbij de geleidingsband (de dichtstbijzijnde energiebandtussenruimte) heeft een hogere elektrische geleidbaarheid dan een metaal X waarin het Fermi niveau verwijderd van de band.
Semiconductors
De elektrische geleidbaarheid bestaat dan uit de migratie van elektronen van een valentieband naar een geleidingsband.
Als de energiekloof tussen beide banden erg groot is, hebben we een isolerende vaste stof (zoals bij B). Aan de andere kant, als deze kloof relatief klein is, is de vaste stof een halfgeleider (in het geval van C).
Geconfronteerd met een toename in temperatuur, verwerven de elektronen in de valentieband voldoende energie om naar de geleidingsband te migreren. Dit resulteert in een elektrische stroom.
In feite is dit een kwaliteit van vaste stoffen of halfgeleidermaterialen: bij kamertemperatuur zijn het isolatoren, maar bij hoge temperaturen zijn het geleiders.
Intrinsieke en extrinsieke halfgeleiders

Intrinsieke geleiders zijn die waarbij de energiekloof tussen de valentieband en de geleidingsband klein genoeg is, zodat de thermische energie de doorgang van elektronen mogelijk maakt.
Aan de andere kant vertonen extrinsieke geleiders veranderingen in hun elektronische structuren na dotering met onzuiverheden, die hun elektrische geleidbaarheid vergroten. Deze onzuiverheid kan een ander metaal of een niet-metaalachtig element zijn.
Indien de verontreiniging meer valentie elektronen, kan een donor band die bruggen elektronen van de valentieband kruising in de geleidingsband te brengen. Deze vaste stoffen zijn halfgeleiders van het n-type. Hier komt de n-aanduiding van "negatief".
In het bovenste plaatje is de donorband afgebeeld in het blauwe blok net onder de rijband (Type n).
Anderzijds, wanneer de onzuiverheid minder valentie elektronen, biedt een acceptor band, waarbij de bandafstand tussen de valentieband en de geleidingsband verkort.
De elektronen migreren eerst naar deze band, waarbij ze achter "positieve gaten" achterblijven, die in de tegenovergestelde richting bewegen.
Omdat deze positieve openingen de doorgang van elektronen markeren, is de vaste stof of het materiaal een p-type halfgeleider..
Voorbeelden van toegepaste bandentheorie
- Leg uit waarom metalen helder zijn: hun mobiele elektronen kunnen straling absorberen in een breed bereik van golflengten wanneer ze naar hogere energieniveaus springen. Vervolgens zenden ze licht uit en keren terug naar lagere niveaus van de rij.
- Kristallijn silicium is het belangrijkste halfgeleidermateriaal. Indien een gedeelte van silicium is gedoteerd met sporen van een element van groep 13 (B, Al, Ga, In, Tl), wordt een p-type halfgeleider. Terwijl als het wordt gedoteerd met een element uit Groep 15 (N, P, As, Sb, Bi) wordt n-type halfgeleider.
- De lichtemitterende diode (LED) is een gezamenlijke halfgeleider p-n. Wat bedoel je? Dat het materiaal beide soorten halfgeleiders heeft, zowel de n als de p. De elektronen migreren van de geleidingsband van de n-type halfgeleider naar de valentieband van de p-type halfgeleider.
referenties
- Whitten, Davis, Peck & Stanley. Chemie. (8e druk). CENGAGE Leren, p 486-490.
- Shiver & Atkins. (2008). Anorganische chemie (Vierde editie., P 103-107, 633-635). Mc Graw Hill.
- Schip C. R. (2016). Bandentheorie van vaste lichamen. Opgehaald op 28 april 2018, van: hyperphysics.phy-astr.gsu.edu
- Steve Kornic (2011). Gaan van obligaties naar bands vanuit het oogpunt van de chemicus. Opgehaald op 28 april 2018, uit: chembio.uoguelph.ca
- Wikipedia. (2018). Extrinsieke halfgeleider. Opgehaald op 28 april 2018, vanaf: en.wikipedia.org
- Byju'S. (2018). Bandentheorie van metalen. Opgehaald op 28 april 2018, uit: byjus.com



